题目内容
【题目】(10分)某无色溶液样品中溶质可能含有NaOH和Na2SO4,某化学小组同学为了确认两种物质是否存在,设计并进行如下探究活动:
【探究方案设计】
为了确定NaOH的存在,设计了如下方案。
张南同学的方案:取溶液样品少许于试管中,向其中滴加无色酚酞溶液,即可确定溶液中溶质是否含NaOH;
小岗同学的方案:取溶液样品少许于试管中,向其中滴加稀盐酸,即可确定溶液中溶质是否含NaOH;
【交流讨论】
经过小组同学讨论认为小岗同学的方案不可以。
请你表明态度,并对小岗同学的方案进行评价(1)_____________________。由此得出结论,用化学实验的方法验证物质的存在,不仅所加试剂与被检验物质能发生化学反应,还需要(2)________,才能验证物质的存在;经过小组同学讨论后重新设计了整体方案,并进行了如下实验。
【探究实验】
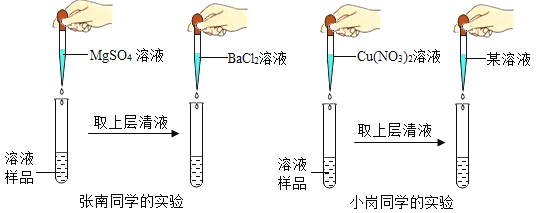
张南同学的实验:重新取溶液样品少许于试管中,向其中滴加足最MgSO4溶液,出现白色沉淀后,取上层清液,再滴加BaCl2溶液,又出现白色沉淀,确定溶液中溶质含NaOH和Na2SO4,请你对张南同学的实验及结论进行评价(3)___________________;小岗同学的实验:重新取溶液样品少许于试管中,其中滴加足量Cu(NO3)2溶液,出现(4) ____________(填实验现象)后,确定溶液中溶质含NaOH,反应的化学方程式为(5)____________;待上述沉淀完全后,取上层清液,再滴加(6) ____________溶液,出现白色沉淀,可确定溶液中溶质含Na2SO4,
【反思与总结】由此得出结论,用化学实验的方法验证同一溶液中两种物质的存在,不仅所加试剂与被检验物质能发生反应,还需要考虑所加试剂(7) ____________,才能验证这两种物质的存在。
【答案】(1)不可以,未滴加指示剂,无法判断NaOH是否与HCl发生反应;
(2)能够检测出反应是否发生;
(3)不能得出结论,因为不严谨,加入的MgSO4溶液也有硫酸根,无法判断检测到的硫酸根是后加入的还是最开始样品中就有的;
(4)蓝色沉淀;
(5)Cu(NO3)2+2NaOH=2NaNO3+Cu(OH)2↓;
(6)BaCl2;
(7)不引入被检测物质。
【解析】
试题分析:(1)酸碱中和反应没有明显现象,需要借助酸碱指示剂才能判断反应是否发生,所以小岗同学的方案不正确,理由是:氢氧化钠与盐酸反应无明显现象,无法确定溶液中是否含有氢氧化钠,由此得出结论,用化学实验的方法验证物质的存在,不仅所加试剂与被检验物质能发生化学反应,还需要有明显的实验现象,才能验证物质的存在;(2)能够检测出反应是否发生;(3) 取溶液样品少许于试管中,向其中滴加足最MgSO4溶液,出现白色沉淀证明溶液中含有NaOH,发生了反应:2NaOH+ MgSO4=Mg(OH)2↓+Na2SO4,取上层清液,再滴加BaCl2溶液,又出现白色沉淀,该沉淀是BaSO4,由于加入的物质中含有SO42-,所以不能确定原溶液是否含有Na2SO4;(4)小岗重新取溶液样品少许于试管中,其中滴加足量Cu(NO3)2溶液,若含有NaOH,会发生反应出现蓝色沉淀;(5)反应的化学方程式是: 2NaOH+ Cu(NO3)2=Cu(OH)2↓+2NaNO3, (6)待上述沉淀完全后,取上层清液,再滴加BaCl2溶液,出现白色沉淀,证明产生了BaSO4沉淀,发生了反应:BaCl2+Na2SO4=BaSO4↓+2NaCl,由此可确定溶液中溶质含Na2SO4;(7)由此得出结论,用化学实验的方法验证同一溶液中两种物质的存在,不仅所加试剂与被检验物质能发生反应,还需要考虑所加试剂不引入被检测物质,才能验证这两种物质的存在。

 小学教材完全解读系列答案
小学教材完全解读系列答案