题目内容
海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、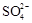 、
、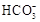 、
、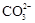 等离子,火力发电时排放的烟气可用海水脱硫,其工艺流程如下图所示:
等离子,火力发电时排放的烟气可用海水脱硫,其工艺流程如下图所示: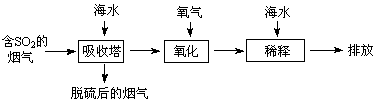
下列说法错误的是
A.海水pH约为8的原因主要是天然海水含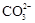 、 、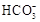 |
B.吸收塔中发生的反应有SO2+H2O H2SO3 H2SO3 |
C.氧化主要是氧气将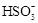 、 、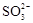 、H2SO3氧化为 、H2SO3氧化为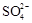 |
D.经稀释“排放”出的废水中,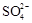 浓度与海水相同 浓度与海水相同 |
D
解析试题分析:A、海水中主要含有Na+、K+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO-3等离子,在这些离子中能发生水解的是CO32-、HCO-3离子,CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-它们水解呈碱性,所以天然海水的pH≈8,呈弱碱性,故A正确;B、天然海水吸收了含硫烟气后,要用O2进行氧化处理,因为氧气具有氧化性,被氧化的硫元素的化合价为+4价,具有还原性,所以氧气将H2SO3、HSO3-、SO32-等氧化为硫酸,如亚硫酸被氧化的反应为2H2SO3+O2=2H2SO4,故B正确;C、氧化后的“海水”需要用大量的天然海水与之混合后才能排放,是因中和稀释经氧气氧化后海水中生成的酸(H+),故C正确;
D、从框图可知:排放”出来的海水,是经过加天然海水中和、稀释经氧化后海水中生成的酸后排放的,溶液的体积显然比进入吸收塔的天然海水大,所以SO42-的物质的量浓度排放出来的海水中浓度小,故D错误。
考点:海水资源及其综合利用;二氧化硫的化学性质

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
下列有关H2SO4的说法中正确的是
| A.将过量的Zn投入一定量的浓H2SO4中,最终生成的气体只有SO2 |
| B.向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 |
| C.运输保存浓硫酸的槽罐车一旦泄露后应立即用大量水冲洗 |
| D.向5 mL 18 mol·L-1的硫酸中加入足量铜片并加热使其充分反应,生成0.045 mol SO2 |
下列说法中正确的是
| A.向久置的氯水中滴入紫色石蕊试液,溶液先变红后褪色 |
| B.纯净的氢气在氯气中安静地燃烧,发出苍白色火焰 |
| C.漂白粉的有效成分是CaCl2和Ca(ClO)2,应密闭保存 |
| D.在氯气泄漏时,可以用浸有NaOH水溶液的毛巾捂住口鼻,并向下风方向跑 |
关于碘及其化合物的说法正确的是
| A.“碘遇淀粉变蓝色”,“碘”指碘元素 |
| B.为了补碘,要多食用含高碘酸的食物 |
| C.I- 与IO3- 可以大量共存于溶液中 |
| D.通过“取样→灼烧→溶解→过滤→萃取”可从海带中提取单质碘 |
下列关于二氧化硫性质的说法正确的是 ( )
| A.氯水中通入一定量二氧化硫气体可增强氯水的漂白性 |
| B.含有酚酞的氢氧化钠溶液中通入二氧化硫气体,溶液变无色,说明二氧化硫具有漂白性 |
| C.二氧化硫既可被氧化也可被还原 |
| D.紫色石蕊试液中通入二氧化硫,溶液先变红后退色 |
下列气体有颜色且有刺激性气味的是( )
| A.NO | B.O2 | C.Cl2 | D.CO |
下列溶液通入过量CO2后,最终溶液中有沉淀析出的是
| A.Na2SO3 | B.BaCl2 | C.Ca(ClO)2 | D.NaAlO2 |
下列有关二氧化硅的叙述中不正确的是
| A.沙子、石英、水晶的主要成分都是SiO2 |
| B.SiO2是制光导纤维的主要原料 |
| C.硅酸可由SiO2直接制得 |
| D.SiO2是酸性氧化物,一定条件下可与碱性氧化物或碱反应 |
氯水中存在多种分子和离子,可通过实验的方法加以确定。下列有关氯水中存在粒子的说法正确的是( )
| A.加入有色布条,一会儿有色布条褪色,证明有Cl2存在 |
| B.溶液呈黄绿色,且有刺激性气味,证明有Cl2分子存在 |
| C.先加入盐酸酸化,再加入AgNO3溶液,产生白色沉淀,证明有Cl-存在 |
| D.加入NaOH溶液,氯水黄绿色消失,证明有HClO分子存在 |