题目内容
科学家致力于二氧化碳的组合转化技术研究,把过多的二氧化碳转化为有益于人类的物质,如将CO2和H2O以1∶4的比例混合,通入反应器,在适当的条件下反应,可获得一种重要的能源。请完成以下化学方程式:CO2+4H2 ( )+2H2O
( )+2H2O
若将二氧化碳与氢气混合,在一定条件下以1∶3的比例发生反应,生成某种重要的化工原料和水,该化工原料可能是( )
 ( )+2H2O
( )+2H2O若将二氧化碳与氢气混合,在一定条件下以1∶3的比例发生反应,生成某种重要的化工原料和水,该化工原料可能是( )
| A.烷烃 | B.烯烃 | C.炔烃 | D.芳香烃 |
CH4 B
从原子守恒的角度去分析,1 mol CO2与4 mol H2反应时,生成了2 mol H2O,生成的另一种物质中必有1 mol C和4 mol H,由方程式的化学计量数可知,此物质必为CH4。同理可知,CO2与H2按物质的量之比1∶3混合,除生成水外,另一种物质的实验式为CH2,也只能为烯烃。?

练习册系列答案
相关题目
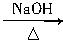 CH3CH2OH+HCl
CH3CH2OH+HCl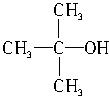 结构相似的醇不能被氧化成醛或羧酸。
结构相似的醇不能被氧化成醛或羧酸。
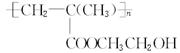 ,它是制作软质隐形眼镜的材料。请写出下列有关反应的化学方程式:
,它是制作软质隐形眼镜的材料。请写出下列有关反应的化学方程式: