题目内容
【题目】已知化合物A中C、H、O三种元素的质量分数分别为37.5%、4.2%和58.3%。请填空:
(1)0.01 mol A在空气中充分燃烧需消耗氧气1.0 L(标准状况),则A的分子式是________。
(2)实验表明:A分子中不含醛基。1 mol A与足量的碳酸氢钠溶液反应可放出3 mol二氧化碳。在浓硫酸催化下,A与乙酸可发生酯化反应。A分子的核磁共振氢谱中有4个吸收峰,且峰面积之比为1∶2∶2∶3。则A的结构简式是____________________。
(3)在浓硫酸催化和适宜的反应条件下,1 mol A与 3 mol乙醇反应生成B,则B的化学式为________,官能团的名称为________,由A生成B的反应类型是____________,该反应的化学方程式是________。
【答案】C6H8O7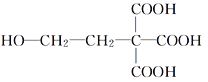 C12H20O7羟基、酯基酯化反应(或取代反应)
C12H20O7羟基、酯基酯化反应(或取代反应)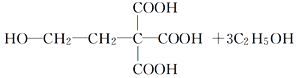
![]()

【解析】
(1)化合物A中C、H、O三种元素的质量分数分别为37.5%、4.2%和58.3%,则N(C):N(H):N(O)=![]() =6:8:7。设A的化学式为(C6H8O7)x,0.01molA在空气中充分燃烧需消耗氧气1.0 L,则0.01x×(6+8/4-7/2)×22.4=1.0,解得x≈1,因此A的化学式为C6H8O7;
=6:8:7。设A的化学式为(C6H8O7)x,0.01molA在空气中充分燃烧需消耗氧气1.0 L,则0.01x×(6+8/4-7/2)×22.4=1.0,解得x≈1,因此A的化学式为C6H8O7;
(2)A中不饱和度为(6×2+2-8)/2=3,说明A中含有三个双键,A中不含醛基,1molA与足量的碳酸氢钠溶液反应可以放出3mol二氧化碳,说明A中含有3个羧基,在浓硫酸催化下,A与乙酸发生酯化反应,说明A中含有羟基;A分子的核磁共振氢谱中有4个吸收峰,且峰面积之比为1∶2∶2∶3,说明A中含有四种类型的氢原子,结合其分子式知,A的结构简式为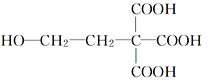 ;
;
(3)A在浓硫酸催化和适宜的反应条件下,1 mol A与 3 mol乙醇反应生成B,该反应是羧基与羟基的酯化反应,B的结构简式为 ,所以B的分子式为C12H20O7,分子中含有的官能团是羟基、酯基,该反应方程式为
,所以B的分子式为C12H20O7,分子中含有的官能团是羟基、酯基,该反应方程式为
![]()
 。
。

 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案