题目内容
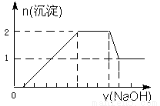
某无色溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42- 等离子中的几种,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。下列说法一定正确的是
A.一定存在H+、Mg2+、Al3+、NH+4,一定不存在Na+、SO2-4、Fe3+
B.一定存在H+、Al3+、NH+4、SO2-4,可能存在Na+、Mg2+
C.溶液中c(H+)∶c(Al3+):c(Mg2+)为1∶1∶1
D.溶液中c(H+)∶c(SO2-4)为2∶9
C
【解析】
试题分析:无色溶液肯定没有三价铁离子。从图象可知,开始时无沉淀产生,说明含有H+,H++OH-=H2O,该氢离子消耗NaOH溶液的体积为1体积,图象中有一段平台,说明加入OH-时无沉淀生成,有NH4+,NH4++OH-=NH3 H2O,铵根消耗氢氧化钠为3体积,最后溶液中有沉淀,说明溶液中含Mg2+,肯定含有Al3+,根据Al3++3 OH-=Al(OH)3↓,铝离子消耗NaOH溶液的体积为3体积,氢氧化铝沉淀溶解消耗1体积氢氧化钠,沉淀的量减小1mol,可知铝离子为1mol。生成2mol沉淀时共消耗5mol的氢氧化钠,其中铝离子占了3mol,还有2mol是镁,镁离子的物质的量为1mol。所以可得到H+、Al3+、Mg2+的物质的量之比为1:1:1。钠离子不能确定有无。选C。

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案
相关题目