题目内容
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固。由此可见( )
A. NH4HCO3和盐酸的反应是放热反应
B.该反应中,热能转化为产物内部的能量
C.反应物的总能量高于生成物的总能量
D.反应的热化学方程式为:NH4HCO3+HCl===NH4Cl+CO2↑+H2O ΔH=+Q
解析:选B 根据醋酸逐渐凝固说明该反应是吸热反应,则A、C错误,B正确,热化学方程式要标出物质的状态,D错误。

 科学实验活动册系列答案
科学实验活动册系列答案化合物A、B是中学常见的物质,其阴阳离子可从下表中选择
| 阳离子 | K+ 、Na+ 、Fe2+ 、Ba2+、NH |
| 阴离子 | OH-、NO |
(1)若A、B的水溶液均为无色,B的水溶液呈碱性,且混合后只产生不溶于稀硝酸的白色沉淀及能使红色石蕊试纸变蓝的气体。
①B的化学式为_________________________________________________________。
②A、B溶液混合后加热呈中性,反应的离子方程式为
________________________________________________________________________。
(2)若A的水溶液呈浅绿色,B的水溶液无色且其焰色反应为黄色。向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合亦无明显变化。则
①A为___________________________________________________________。
②经分析上述过程中溶液变黄的原因可能有两种:
Ⅰ.________________________________________________________________________。
Ⅱ.________________________________________________________________________。
③请用一简易方法证明上述溶液变黄的原因__________________________________。
④利用溶液变黄原理,将其设计成原电池,若电子由a流向b,则b极的电极反应式为
______________________________________________________________________ __
__
________________________________________________________________________。
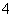
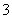 、I-、HCO
、I-、HCO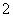 、HSO
、HSO 接钢轨,请写出反应的化学方程式:________________________________________________________________________。
接钢轨,请写出反应的化学方程式:________________________________________________________________________。 ___________________________________________________
___________________________________________________ _______________________________________。
_______________________________________。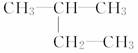 ______________________________________________;
______________________________________________;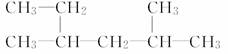 ___________________________________;
___________________________________;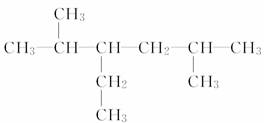 _______________________________;
_______________________________;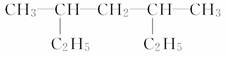 ___________________________________;
___________________________________;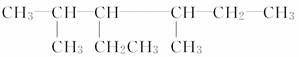 __________________________。
__________________________。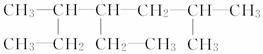 的名称为____________________。
的名称为____________________。 ”基团,则其可能的结构简式为________________________________(任写一种)。
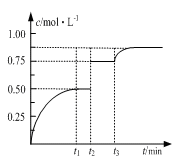
”基团,则其可能的结构简式为________________________________(任写一种)。  xP(g)+Q(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体P的浓度随时间变化如图所示。下列说法正确的是( )
xP(g)+Q(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体P的浓度随时间变化如图所示。下列说法正确的是( )