题目内容
【题目】下列共价键①H-H、②H-F、③H-O、④N-H、⑤P-H中,键的极性由小到大的顺序正确的是 ( )
A. ①②③④⑤B. ⑤④③②①C. ①⑤④③②D. ②③④⑤①
【答案】C
【解析】
对于元素周期表中,同周期的元素从左到右原子半径减小,原子核对外层电子的引力增强,与氢元素形成共价键时极性增强,则极性由小到大分别是N-H、H-O、H-F;
同主族的元素从上到下原子半径增大,原子核对外层电子的引力减弱,与氢元素形成共价键时极性减弱,对于第ⅤA族的元素,与氢元素形成共价键时,极性:N-H大于P-H;H-H键属于非极性键,极性由小到大的顺序为:①⑤④③②。
故选C。

 小学期末标准试卷系列答案
小学期末标准试卷系列答案【题目】将不可再生的天然气、石油、煤等化石燃料转化利用、变废为宝已成为当务之急.
(1)根据键能数据估算CH4+4F2=CF4+4HF的反应热△H= .
化学键 | C﹣H | C﹣F | H﹣F | F﹣F |
键能/(kJmol﹣1) | 414 | 489 | 565 | 155 |
(2)甲醇、二甲醚(CH3OCH3)被称为21世纪的新型燃料,均可利用CO和H2反应合成.
①某燃料电池以二甲醚为原料,熔融碳酸盐为电解质,其负极反应如下:CH3OCH3+6CO ![]() ﹣12e﹣=8CO2+3H2O.写出该燃料电池的正极反应式: .
﹣12e﹣=8CO2+3H2O.写出该燃料电池的正极反应式: .
②废水中含甲醇对水质会造成污染,Co3+可将甲醇氧化为CO2 . 某同学以Pt作电极电解酸性含甲醇废水与CoSO4混合液模拟工业除污原理,其阳极反应式为 .
(3)某企业采用如图所示原理处理化石燃料开采、加工过程产生的H2S废气.
①电解池中电极A、B均为惰性电极,其中A为电解池的极;电极B所得到的物质X的分子式为 .
②反应池中发生的离子反应方程式为 . 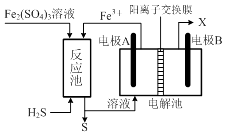
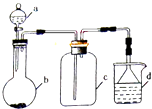
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持、加热和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓硝酸 | Cu | NO2 | NaOH溶液 |
B | 浓氨水 | CaO | NH3 | H2O |
C | 稀硝酸 | Cu | NO | H2O |
D | 浓硫酸 | Cu | SO2 | 饱和NaHSO3溶液 |
A.A
B.B
C.C
D.D