��Ŀ����
ij��Ȼ����Ʒ����ɿ���ΪaNa2CO3•bNaHCO3•cH2O��a��b��cΪ����������Ϊȷ������ɣ�ijС���������ʵ�飺
��1������ʵ��
��ȡ������Ȼ����Ʒ�����Թ��У��þƾ��Ƽ��ȣ����Թܿ���Һ�����ɣ���Һ����ʹ��ˮ����ͭ������___________����ܡ����ܡ���˵����Ʒ�к��ᾧˮ���Լ������� ��
�������һ��������ȷ����Ʒ�к���CO32��  ��
��
��2����������
��ͬѧ���������ͼ��ʾװ�ã��ⶨ��Ȼ��Ļ�ѧ��ɡ�
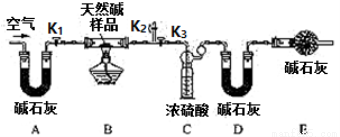
ʵ�鲽�裺
����װ��ʵ��װ�ú����Ƚ��еIJ����� ��A����ʯ�ҵ������ǣ�E����ʯ�ҵ������� ��
�ڳ�7.3g��Ʒ������Ӳ�ʲ������У�����Cװ������Ϊ87.6g��Dװ��Ϊ74.7g��
�۴���K1��K2���ر�K3��ͨ����������ӡ�
�ܹرջ���Kl��K2����K3����ȼ�ƾ��������ٲ�������Ϊֹ��
�ݴ���Kl��������������ӣ�Ȼ��Ƶ�Cװ������Ϊ88.5g��Dװ������Ϊ75.8g��ͨ�������Ŀ���� ��
�����a=1�������Ȼ��Ļ�ѧʽΪ ��
һ���¶��£������������Ϊ2.0L�ĵĺ����ܱ������з������·�Ӧ��PCl5(g) PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
��� | �¶ȣ��棩 | ��ʼ���ʵ�����mol�� | ƽ�����ʵ�����mol�� | �ﵽƽ������ʱ��s�� | |
PCl5��g�� | PCl3��g�� | Cl2��g�� | |||
�� | 320 | 0.40 | 0.10 | 0.10 | t1 |
�� | 320 | 0.80 | t2 | ||
�� | 410 | 0.40 | 0.15 | 0.15 | t3 |
����˵����ȷ����
A��ƽ�ⳣ��K��������>������
B����Ӧ����ƽ��ʱ��PCl5��ת���ʣ�������>������
C����Ӧ����ƽ��ʱ������I�е�ƽ������Ϊv(PCl5)=0.1/t1 mol/(L��s)
D����ʼʱ���������г���PCl5 0.30 mol��PCl3 0.45 mol��Cl2 0.10 mol����Ӧ�����淴Ӧ�� �����
�����


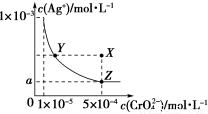
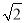 ��10��4
��10��4