题目内容
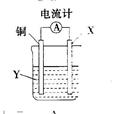
某小组为研究电化学原理,设计如图装置,下列叙述正确的是
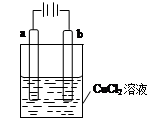

| A.若a和b为石墨,通电后a电极上发生的反应为2Cl--2e-=Cl2↑ |
| B.若a和b为石墨,通电后b电极上发生氧化反应 |
| C.若a为铜,b为铁,通电后a电极质量增加 |
| D.若a为铜,b为铁,通电后Cu2+向铁电极移动 |
AD
试题分析:读图可知,该装置为电解池,与电源正极相连的a电极为阳极,氯化铜溶液中的氯离子和氢氧根离子移向阳极,由放电顺序可知氯离子在a电极上发生氧化反应,失去电子变成氯气,故A正确;与电源负极相连的b电极为阴极,阴极上发生还原反应,故B错误;依题意可知,该装置为电镀池,Cu作阳极,由于铜电极不是惰性电极,则阳极反应式为Cu-2e-=Cu2+,则通电后a电极的质量减小,故C错误;与电源负极相连的铁电极为阴极,则溶液中的阳离子移向铁电极,由放电顺序可知,阴极反应式为Cu2++2e-=Cu,故D正确。

练习册系列答案
相关题目