题目内容
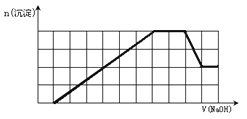
【题目】将一定量的铝粉、氧化铝、氧化镁的混合物加入到300mL4mol/L的稀硫酸中,生成标准状况下6.72L气体。向反应后的溶液中滴加一定物质的量浓度的KOH溶液时,所得沉淀的物质的量(mol)与滴加KOH溶液的体积(mL)之间的关系如图所示:

(1)OA对应反应的离子方程式为________________,BC对应反应的离子方程式为_________________;
(2)c(KOH)=_________mol/L,混合物中氧化铝的物质的量为_____mol;
(3)A点对应的数值为_______;
(4)在中学阶段,实验室里检验B点对应的溶液中的阳离子时,所观察到的现象是___________。
(5)向C点对应的溶液中通入足量的CO2所发生反应的离子方程式为__________________。
【答案】 H+ +OH-=H2O Al(OH)3 +OH-=AlO2-+2H2O 4 0.1 200 透过蓝色钴玻璃观察,火焰呈紫色 CO2 +AlO2- +2H2O=Al(OH)3↓+HCO3-
【解析】将一定量的铝粉、氧化铝、氧化镁的混合物加入到300mL4mol/L的稀硫酸中,生成标准状况下6.72L气体,氢气的物质的量为![]() 0.3mol,根据2Al~~3H2,混合中Al粉的物质的量为0.3mol×
0.3mol,根据2Al~~3H2,混合中Al粉的物质的量为0.3mol×![]() =0.2mol;向反应后的溶液中滴加一定物质的量浓度的KOH溶液时,根据沉淀的物质的量(mol)与滴加KOH溶液的体积(mL)之间的关系图,可知:(1)OA段酸过量,发生酸碱中和反应,离子反应方程式为H+ +OH-=H2O;继续滴加KOH溶液将溶液里的Al3+和Mg2+转化为Al(OH)3和Mg(OH)2沉淀,BC段滴加KOH溶液,溶解生成的Al(OH)3沉淀,发生反应的离子方程式为Al(OH)3 +OH-=AlO2-+2H2O;
=0.2mol;向反应后的溶液中滴加一定物质的量浓度的KOH溶液时,根据沉淀的物质的量(mol)与滴加KOH溶液的体积(mL)之间的关系图,可知:(1)OA段酸过量,发生酸碱中和反应,离子反应方程式为H+ +OH-=H2O;继续滴加KOH溶液将溶液里的Al3+和Mg2+转化为Al(OH)3和Mg(OH)2沉淀,BC段滴加KOH溶液,溶解生成的Al(OH)3沉淀,发生反应的离子方程式为Al(OH)3 +OH-=AlO2-+2H2O;
(2)B点为完全沉淀点,此时溶液中溶质K2SO4,根据原子守恒可知n(K+)=2n(SO42-)=2×0.3L×4mol/L=2.4mol,此时消耗KOH溶液体积为0.6L,则c(KOH)=![]() =4mol/L;BC段共消耗KOH溶液体积为0.1L,根据Al(OH)3 +OH-=AlO2-+2H2O可知Al(OH)3 的物质的量为4mol/L×0.1L=0.4mol;设氧化铝的物质的量为n mol,根据原子守恒2n mol+0.2 mol=0.4mol,n=0.1;
=4mol/L;BC段共消耗KOH溶液体积为0.1L,根据Al(OH)3 +OH-=AlO2-+2H2O可知Al(OH)3 的物质的量为4mol/L×0.1L=0.4mol;设氧化铝的物质的量为n mol,根据原子守恒2n mol+0.2 mol=0.4mol,n=0.1;
(3)C点对应的沉淀Mg(OH)2物质的量为 0.2mol,则生成沉淀Mg(OH)2和Al(OH)3 消耗KOH的物质的量为0.2mol×2+0.4mol×3=1.6mol,消耗KOH溶液的体积为![]() =400mL,则A点对应的数值为600mL-400mL=200mL;
=400mL,则A点对应的数值为600mL-400mL=200mL;
(4)K+的检验可用焰色反应,具体操作是透过蓝色钴玻璃观察,火焰呈紫色;
(5)C点对应的溶液中含有AlO2-,通入足量的CO2所发生反应的离子方程式为CO2 +AlO2- +2H2O=Al(OH)3↓+HCO3-;

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案