题目内容
【题目】代沟是化学老师说什么你都不听,代价就是这道题你什么都不会!
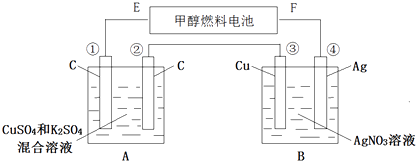
I. A、B、C、D四种物质均含有同一种元素。A是常见的金属单质,C的水溶液呈黄色。A、B、C、D之间在一定条件下有如图所示转化关系:

请回答下列问题:
(1)A的化学式是_____________________。
(2)反应①的反应类型为_____________反应(选填“化合”、“分解”、“置换”、“复分解”)。
(3)反应②的化学方程式是___________________________。
(4)C的水溶液与NaOH溶液混合后发生反应的离子方程式是______________________。
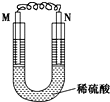
II. 实验室可以用如图所示装置制取乙酸乙酯。请回答下列问题:

(1)a试管中盛放的是饱和碳酸钠溶液,制得的乙酸乙酯在饱和碳酸钠溶液的________(填“上”或“下”)层。
(2)制取乙酸乙酯的化学方程式是________________,该反应属于_______________反应(填反应类型)。左边试管中在加热前往往加入 ____________以用于防爆沸。
【答案】 Fe 置换 2FeCl2 + Cl2 = 2FeCl3 Fe3++3OH- = Fe(OH)3↓ 上 CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O 酯化反应或取代反应 碎瓷片
CH3COOCH2CH3+H2O 酯化反应或取代反应 碎瓷片
【解析】I.A是常见的金属,与氯气反应生成C,C的溶液呈现黄色,且C与KSCN溶液混合溶液为血红色,则C含有Fe3+,由元素守恒可以知道A为Fe,结合转化关系可以知道,C为FeCl3,B为FeCl2,以此解答该题。
II.该实验为乙酸乙酯的制备实验,乙酸和乙醇在浓硫酸作用下发生酯化反应生成乙酸乙酯,乙酸乙酯密度比水小,不溶于水,常用饱和碳酸钠溶液对乙酸乙酯进行分离提纯;为了防止加热时出现暴沸,常加入碎瓷片;据此分析解答问题。
(1)由上述分析可以知道,A为Fe;正确答案:Fe。
(2)铁与盐酸反应生成氯化亚铁和氢气,为置换反应;正确答案:置换。
(3)氯化亚铁与氯气反应生成氯化铁,化学方程式是2FeCl2+Cl2 =2FeCl3;正确答案:2FeCl2+Cl2 =2FeCl3。
(4)氯化铁溶液与NaOH溶液反应生成氢氧化铁红褐色沉淀,离子方程式是:Fe3++3OH- = Fe(OH)3↓;正确答案:Fe3++3OH- = Fe(OH)3↓。
II. (1)乙酸乙酯的密度小于水的密度,不溶于水,所以制得的乙酸乙酯在饱和碳酸钠溶液的上层;正确答案:上。
(2)乙醇和乙酸在浓硫酸作催化剂条件下发生酯化反应生成乙酸乙酯和水,化学方程式是:CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O ;该反应属于取代反应或酯化反应;左边试管中在加热前往往加入碎瓷片以用于防爆沸;正确答案:CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O ;该反应属于取代反应或酯化反应;左边试管中在加热前往往加入碎瓷片以用于防爆沸;正确答案:CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O ;酯化反应或取代反应; 碎瓷片。
CH3COOCH2CH3+H2O ;酯化反应或取代反应; 碎瓷片。

【题目】下表是两种生物干重中有关元素的质量分数(%)。根据下表,有人得出下面结论,其中正确的是( )
元素 | C | H | O | N | P | S |
生物甲 | 43.57 | 6.24 | 44.43 | 1.46 | 0.20 | 0.17 |
生物乙 | 55.99 | 7.46 | 14.62 | 9.33 | 3.11 | 0.78 |
A.如果它们分别是动物和植物,则甲是动物,乙是植物
B.甲生物可能含有叶绿素
C.两者体细胞中,甲有细胞核乙没有细胞核
D.两者的含水量比较,可推测甲比乙多