题目内容
(10分)在铜片、锌片和200 mL稀硫酸组成的原电池中,若电路中通过0.3 mol e—,H2SO4恰好作用完毕。试计算:
(1)所消耗锌的质量;
(2)生成气体的体积(在标准状况下);
(3)原200 mL稀硫酸的物质的量浓度。
(1)所消耗锌的质量;
(2)生成气体的体积(在标准状况下);
(3)原200 mL稀硫酸的物质的量浓度。
(1)9.75g (2)3.36L (3)0.75mol/L
考查原电池的有关计算。
(1)锌比铜活泼,所以锌是负极,电极反应式为Zn-2e-=Zn2+
所以消耗锌是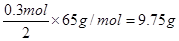 。
。
(2)正极是氢离子得到电子,电极反应式为2H++2e-=H2↑
所以标准状况下氢气的体积是
(3)根据氢原子守恒可知,硫酸的浓度是 。
。
(1)锌比铜活泼,所以锌是负极,电极反应式为Zn-2e-=Zn2+
所以消耗锌是
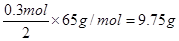 。
。(2)正极是氢离子得到电子,电极反应式为2H++2e-=H2↑
所以标准状况下氢气的体积是

(3)根据氢原子守恒可知,硫酸的浓度是
 。
。
练习册系列答案
相关题目






 AsO33-+I2+H2O,设计如下图装置,进行下述操作:
AsO33-+I2+H2O,设计如下图装置,进行下述操作: