题目内容
【题目】某兴趣小组对物质的性质进行相关探究. 【提出问题】氯化氢(HCl)气体显酸性吗?
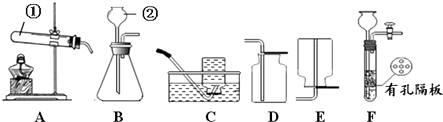
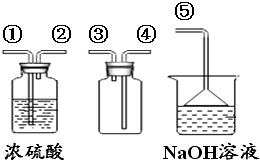
【进行实验】该兴趣小组的同学根据二氧化碳与水反应的实验探究方法,用三朵由紫甘蓝的汁液染成蓝紫色的纸质干燥小花进行如图1的三个实验:
实验现象:Ⅰ和Ⅱ中小花不变色;Ⅲ中小花变红色.
【查阅资料】图2是同学们查阅的氯化氢气体溶于水的微观示意图.
【实验结论】氯化氢气体不显酸性.
【交流反思】
(1)从微观角度分析氯化氢气体不显酸性的原因是 .
(2)小明向实验Ⅲ中变红的小花上喷适当过量的稀氢氧化钠溶液,发现小花最后变成黄绿色,写出相关反应的化学方程式 .
(3)紫甘蓝的汁液在酸性溶液中显色,在碱性溶液中显色.
(4)下列实验可以用来说明氯化氢气体不显酸性的是 .
A.测试盐酸的导电性,盐酸能导电
B.干燥的碳酸钠粉末放人氯化氢气体中,不反应
C.氢气与氯气反应,生成氯化氢气体
D.干燥的碳酸钠粉末放人盐酸中,能反应.
【答案】
(1)在氯化氢气体中,氯化氢以分子形式存在,没有解离出氢离子,所以氯化氢气体不显酸性
(2)NaOH+HCl=NaCl+H2O
(3)红;黄绿
(4)B
【解析】解:(1)在氯化氢气体中,氯化氢气体是由氯化氢分子构成的,没有解离出的氢离子,所以氯化氢气体不显酸性, 所以答案是:在氯化氢气体中,氯化氢气体是由氯化氢分子构成的,没有解离出的氢离子,所以氯化氢气体不显酸性;(2)稀氢氧化钠溶液和盐酸反应生成氯化钠和水,所以向实验Ⅲ中变红的小花上喷足量的稀氢氧化钠溶液,发现小花最后变成黄绿色,反应的化学方程式NaOH+HCl=NaCl+H2O,
所以答案是:NaOH+HCl=NaCl+H2O;(3)由图可知紫甘蓝的汁液在酸性溶液中显红色,在碱性溶液中显黄绿色,
所以答案是:红,黄绿色;(4)碳酸钠粉末遇到酸性物质会生成二氧化碳,所以干燥的碳酸钠粉末放入氯化氢气体中,不反应,说明氯化氢气体不显酸性,
所以答案是:B.

【题目】如图所示,将少量液体X加入到烧瓶中,观察到气球逐渐膨胀.如表中液体X和固体Y的组合,不符合题意的是( )
① | ② | ③ | ④ | |
X | 水 | 水 | 稀硫酸 | 双氧水 |
Y | 硝酸铵 | 氢氧化钠 | 氯化钠 | 二氧化锰 |

A.①③
B.②④
C.①②
D.③④
【题目】某温度下,H2(g) + CO2(g) ![]() H2O(g)+ CO(g)的平衡常数K=9/4。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和 CO2(g),其起始浓度如下表所示
H2O(g)+ CO(g)的平衡常数K=9/4。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和 CO2(g),其起始浓度如下表所示
起始浓度 | 甲 | 乙 | 丙 |
C(H2)/ mol·l-1 | 0.010 | 0.020 | 0.020 |
C(CO2)/ mol·l-1 | 0.010 | 0.010 | 0.020 |
下列判断不正确的是
A. 平衡时,乙中CO2 的转化率大于60%
B. 平衡时,甲和丙中H2 的转化率均是60%
C. 平衡时,丙中C(CO2)是甲中的2倍,是0.012 mol·l-1
D. 反应开始时,丙中的反应速率最快,甲中的反应速率最慢