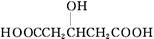题目内容
将含有C、H、O的有机物3.0g装入元素分析装置,通入足量的O2使之完全燃烧,将生成的气体依次通过装有CaCl2(A)和碱石灰(B)的干燥管,测得A管质量增加了1.8 g,B管质量增加了4.4 g,已知该有机物的相对分子质量为60。(1)燃烧此有机物3.0 g需消耗O2(标准状况) L;(2)求此有机物的分子式 。
(1)2.24L (2)C2H4O2
试题分析:(1)根据质量守恒定律可知燃烧此有机物3.0 g需消耗O2的质量为1.8 g +4.4 g -3.0g =3.2g.n(O2)=3.2g÷32g/mol=0.1mol.所以在标准状况下其体积为2.24L。(2)n(H2O)= 1.8 g÷ 18g/mol= 0.1mol;n(CO2)= 4.4 g÷44g/mol=0.1mol。所以在3.0g该有机物中,含有H:0.2mol;C:0.1mol;O:(3.0g-0.2mol×1g/mol-0.1mol×12g/mol)÷16g/mol=0.1mol。所以该化合物的最简式是CH2O,其式量为30. 因为该有机物的相对分子质量为60。所以该化合物的分子式为C2H4O2。

练习册系列答案
相关题目
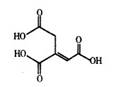
 CHCOOH
CHCOOH