题目内容
在一定温度下将各1mol CO和水蒸气放在密闭的容器中反应:CO(g)+H2O(g) CO2(g)+ H2(g)达到平衡后,测得CO2为0.6mol,再通入4mol水蒸气,达到平衡后CO2的物质的量为
CO2(g)+ H2(g)达到平衡后,测得CO2为0.6mol,再通入4mol水蒸气,达到平衡后CO2的物质的量为
 CO2(g)+ H2(g)达到平衡后,测得CO2为0.6mol,再通入4mol水蒸气,达到平衡后CO2的物质的量为
CO2(g)+ H2(g)达到平衡后,测得CO2为0.6mol,再通入4mol水蒸气,达到平衡后CO2的物质的量为| A.等于0.6mo | B.等于1mol |
| C.大于0.6mol小于1mol | D.大于1mol |
C
首先,再次达到平衡时各物质都存在,假设CO完全转化为CO2,则有CO21mol,但平衡时有CO存在,故CO2小于1mol.看第一次达到平衡时,CO2为0.6mol,加入4mol水蒸气后,根据勒夏特列原理,平衡正向移动,所以CO2要大于0.6mol。故答案选C

练习册系列答案
相关题目
 N的键能是946 kJ/mol,H—H的键能为436 kJ/mol,N—H的键能为391 kJ/mol,请据此写出合成氨反应的热化学方程式 ;
N的键能是946 kJ/mol,H—H的键能为436 kJ/mol,N—H的键能为391 kJ/mol,请据此写出合成氨反应的热化学方程式 ; 2NO(g)的平衡常数K如下表:
2NO(g)的平衡常数K如下表: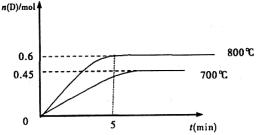
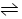 4C(g)达到平衡时 C的浓度为1.2 mol·L-1,当其它条件不变,把体积扩大1倍时,测得C的浓度为0.7 mol·L-1,则x的值为 ( )
4C(g)达到平衡时 C的浓度为1.2 mol·L-1,当其它条件不变,把体积扩大1倍时,测得C的浓度为0.7 mol·L-1,则x的值为 ( ) x Z(g) ΔH<0
x Z(g) ΔH<0 2NH3。已知平衡时NH3的浓度是c mol·L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol·L-1的是
2NH3。已知平衡时NH3的浓度是c mol·L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol·L-1的是 2SO3(g);△H=-akJ·mo1-2在相同条件下要想得到2akJ热量,加入各物质的物质的量可能是( )
2SO3(g);△H=-akJ·mo1-2在相同条件下要想得到2akJ热量,加入各物质的物质的量可能是( ) 2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图:
2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图: