题目内容
【题目】Mg﹣AgCl电池是一种以海水为电解质溶液的水激活电池.下列叙述正确的是( )
A.正极反应式为Mg﹣2e﹣═Mg2+
B.正极反应式为Ag+e﹣═Ag
C.电池放电时Cl﹣由负极向正极迁移
D.负极会发生副反应Mg+2H2O═Mg(OH)2+H2↑
【答案】D
【解析】解:A.活泼金属镁作负极,失电子发生氧化反应,反应式为:Mg﹣2e﹣=Mg2+ , 故A错误;
B.AgCl是难溶物,其电极反应式为:2AgCl+2e﹣═2C1﹣+2Ag,故B错误;
C.原电池放电时,阴离子向负极移动,则Cl﹣在正极产生由正极向负极迁移,故C错误;
D.镁是活泼金属与水反应,即Mg+2H2O=Mg(OH)2+H2↑,故D正确;
故选:D.

 名校课堂系列答案
名校课堂系列答案【题目】下列各组物质中,物质之间通过一步反应就能实现如图所示变化的是( )
选项 | 甲 | 乙 | 丙 | 丁 |
A | N2 | NH3 | NO | NO2 |
B | Na | Na2O | NaOH | Na2O2 |
C | SiO2 | SiF4 | H2SiO3 | Na2SiO3 |
D | Al | AlCl3 | Al2O3 | NaAlO2 |

A.A
B.B
C.C
D.D
【题目】由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、Cl﹣、NH4+、Mg2+、Ba2+、CO32﹣、SO42﹣ , 将该混合物溶于水后得澄清溶液,现取3份100mL 的该溶液分别进行如下实验:
实验序号 | 实验内容 | 实验结果 |
① | 加AgNO3溶液 | 有白色沉淀生成 |
② | 加足量NaOH溶液并加热 | 收集到气体1.12L(标准状况) |
③ | 加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加入足量稀盐酸,然后干燥、称量 | 第一次称量读数为6.27g;第二次称量读数为2.33g |
试回答下列问题:
(1)根据实验①对Cl﹣是否存在的判断是(填“一定存在”、“一定不存在”或“不能确定”),根据实验①②③判断混合物中一定不存在的离子是 .
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满)
阴离子符号 | 物质的量浓度(molL﹣1) |
(3)试确定K+是否存在并说明理由.
【题目】工业上用菱锰矿(MnCO3)[含FeCO3、SiO2、Cu2(OH)2CO3等杂质]为原料制取二氧化锰,其流程示意图如下: 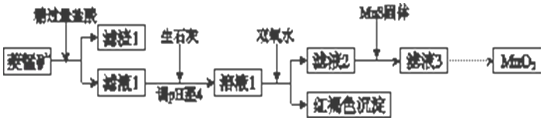
已知:
生成氢氧化物沉淀的pH
Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
开始沉淀时 | 8.3 | 6.3 | 2.7 | 4.7 |
完全沉淀时 | 9.8 | 8.3 | 3.7 | 6.7 |
注:金属离子的起始浓度为0.1mol/L
回答下列问题:
(1)含杂质的菱锰矿使用前需将其粉碎,主要目的是 . 盐酸溶解MnCO3的化学方程式是 .
(2)向溶液1中加入双氧水时,反应的离子方程式是 .
(3)滤液2中加入稍过量的难溶电解质MnS,以除去Cu2+ , 反应的离子方程式是 .
(4)将MnCl2转化为MnO2的一种方法是氧化法.其具体做法是用酸化的NaClO3溶液将MnCl2氧化,该反应的离子方程式为: Mn2++ClO3﹣+=++ .
(5)将MnCl2转化为MnO2的另一种方法是电解法. ①生成MnO2的电极反应式是
②若直接电解MnCl2溶液,生成MnO2的同时会产生少量Cl2 . 检验Cl2的操作是 .
③若在上述MnCl2溶液中加入一定量的Mn(NO3)2粉末,则无Cl2产生.其原因是 .
