题目内容
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
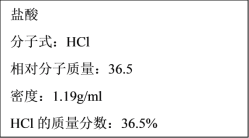
(1)该浓盐酸的物质的量浓度为___mol·L-1。
(2)某学生欲用上述浓盐酸和蒸馏水配制500ml物质的量浓度为0.4mol·L-1的稀盐酸,该学生需用量筒量取___ml上述浓盐酸进行配制。
(3)实验室用盐酸的浓溶液与高锰酸钾发生反应的化学方程式为:2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O,该反应中的氧化剂是___,还原剂是___。(填化学式)
【答案】11.9 16.8 KMnO4 HCl
【解析】
(1)质量分数36.5%,密度为1.19g/mL的盐酸的物质的量浓度c= ![]() ;
;
(2)配制450mL物质的量浓度为0.4molL-1的稀盐酸,设需要浓盐酸体积为V,则依据溶液稀释规律,V×11.9mol/L=0.4mol/L×500mL,解得V;
(3)2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O中,Mn元素化合价降低,是氧化剂;Cl元素化合价升高,是还原剂。
(1)质量分数36.5%,密度为1.19g/mL的盐酸的物质的量浓度c= ![]() =
= ![]() mol/L=11.9mol/L;故答案为:11.9;
mol/L=11.9mol/L;故答案为:11.9;
(2)配制450mL物质的量浓度为0.4molL-1的稀盐酸,由于实验室没有450mL的容量瓶,所以需要选择500mL的容量瓶,配制成500mL溶液,设需要浓盐酸体积为V,则依据溶液稀释规律,V×11.9mol/L=0.4mol/L×500mL,解得V=16.8mL;
(3)2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O中,Mn元素化合价降低,是氧化剂;Cl元素化合价升高,是还原剂;故答案为:KMnO4;HCl。