题目内容
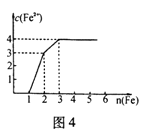
向含有1 mol HNO3和1mol H2SO4的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。下列有关判断不正确的是


| A.a表示Fe3+的关系曲线 |
| B.n1=0.75 |
| C.P点时,n(Fe2+)="0.5625" mol |
| D.向P点溶液中加入铜粉,最多可溶解14.4 g |
C
该反应可以看做二步①Fe+4H++ NO=Fe3++NO↑+2H2O;硝酸根过量,氢离子不足;②2Fe3++Fe=3Fe2+;故A、正确,a表示Fe3+;B、正确,3molH+反应,消耗铁为0.75mol;C、P点二价铁等于三价铁,均为0.45mol,C错误。D、与0.45molFe3+反应,消耗0.225mol铜,质量为14.4g。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 。用此溶液进行以下实验:
。用此溶液进行以下实验: 应的化学方程式:
应的化学方程式: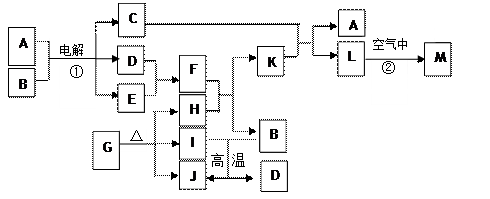
 ,M的化学式 ;
,M的化学式 ;