题目内容
对于可逆反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )分析:根据化学平衡状态的特征分析,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、质量、体积分数以及百分含量不变,以及由此衍生的一些量也不发生变化,本题中从压强对反应速率的影响角度分析体积变化时正逆反应速率的变化.
解答:解:A、反应速率之比等于化学计量数之比,则3V正(NH3)=2V正(H2O),故A错误;
B、反应达到平衡状态时,正逆反应速率相等,4V正(O2)=5V逆(NO),说明消耗氧气的速率和生成氧气的速率相等,故B正确;
C、达到化学平衡时,若增加容器体积,容器的压强减小,正逆反应速率都减小,故C错误;
D、无论是否达到平衡状态,反应速率之比都等于化学计量数之比,即位时间内生成xmolNO的同时,消耗xmolNH3,但不能说明正逆反应速率相等,故D错误.
故选B.
B、反应达到平衡状态时,正逆反应速率相等,4V正(O2)=5V逆(NO),说明消耗氧气的速率和生成氧气的速率相等,故B正确;
C、达到化学平衡时,若增加容器体积,容器的压强减小,正逆反应速率都减小,故C错误;
D、无论是否达到平衡状态,反应速率之比都等于化学计量数之比,即位时间内生成xmolNO的同时,消耗xmolNH3,但不能说明正逆反应速率相等,故D错误.
故选B.
点评:本题考查化学平衡状态的判断,题目难度中等,注意用不同物质的表示的正逆反应速率相等的表达方法,此为易错点.

练习册系列答案
相关题目
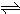
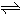 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )