题目内容
【题目】A~G是几种烃的分子球棍模型(如图),据此回答下列问题:
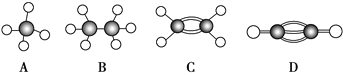
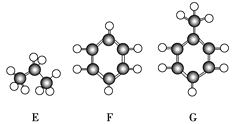
(1)常温下含碳量最高的气态烃是________(填字母)。
(2) E的一氯取代物同分异构有_______种。
(3)一卤代物种类最多的是________(填写字母)。
(4) 能够发生加成反应的烃有________(填写字母)。
(5)写出C的加聚反应的化学方程式:______________________。
【答案】 D 2 4 G 略
【解析】根据结构模型可知A为甲烷,B为乙烷,C为乙烯,D为乙炔,E为丙烷,F为苯,G为甲苯。
(1)常温下,分子中含有碳原子个数不大于4的烃为气态烃,根据其球棍模型判断,分子中含有碳氢原子个数比最大即为含碳量最高的,所以含碳量最大的是乙炔,故答案为:D;
(2) 丙烷分子中含有2种化学环境的氢原子,一氯取代物有2种,故答案为:2;
(3)甲烷、乙烷、乙烯、乙炔、苯的一卤代物都只有1种,丙烷的一卤代物有2种,甲苯的有一卤代物有4种,故答案为:G;
(4)含有碳碳双键或三键或苯环的烃能发生加成反应,所以乙烯、乙炔、苯和甲苯都能发生加成反应, 故答案为:CDFG;
(5)乙烯分子间发生加成聚合反应生成高分子化合物聚乙烯;反应的化学方程式为:![]() ;故答案为:
;故答案为:![]() 。
。

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目