题目内容
【题目】氨气电子式:_______,其分子空间构型是_______,氨气溶于水,溶液呈____性,原因是______(用化学方程式解释)。用玻璃棒蘸浓盐酸接触氨气时,观察到的现象为_____,发生的反应是(用化学方程式表示)________。
【答案】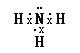 三角锥形 碱 NH3+H2ONH3H2ONH4++OH- 生成白烟 NH3 + HCl=NH4Cl
三角锥形 碱 NH3+H2ONH3H2ONH4++OH- 生成白烟 NH3 + HCl=NH4Cl
【解析】
氨气分子中氮原子和每个H原子之间都存在一对共用电子对;根据价层电子对互斥理论确定氨气的空间构型;氨气溶于水,溶于水的氨气能够和水反应生成一水合氨,一水合氨能够电离出铵根离子和氢氧根离子,据此分析解答。
氨气分子中氮原子和每个H原子之间都存在一对共用电子对,且N原子还有一个孤电子对,氨气的电子式为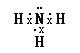 ;氨气分子中氮原子的价层电子对数是4,且含有一个孤电子对,所以其空间构型为三角锥形;氨气溶于水,溶于水的氨气能够和水反应生成一水合氨,一水合氨能够电离出铵根离子和氢氧根离子,导致氨水呈碱性,NH3+H2ONH3H2ONH4++OH-;用玻璃棒蘸浓盐酸接触氨气时,氨气能够与挥发出来的氯化氢化合生成氯化铵固体,因此看到的现象为白烟,NH3 + HCl=NH4Cl,故答案为:
;氨气分子中氮原子的价层电子对数是4,且含有一个孤电子对,所以其空间构型为三角锥形;氨气溶于水,溶于水的氨气能够和水反应生成一水合氨,一水合氨能够电离出铵根离子和氢氧根离子,导致氨水呈碱性,NH3+H2ONH3H2ONH4++OH-;用玻璃棒蘸浓盐酸接触氨气时,氨气能够与挥发出来的氯化氢化合生成氯化铵固体,因此看到的现象为白烟,NH3 + HCl=NH4Cl,故答案为: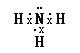 ;三角锥形;碱;NH3+H2ONH3H2ONH4++OH-;生成白烟;NH3 + HCl=NH4Cl。
;三角锥形;碱;NH3+H2ONH3H2ONH4++OH-;生成白烟;NH3 + HCl=NH4Cl。

【题目】A~E是核电荷数均小于20的元素,其结构或性质信息如表:
元素 | A | B | C | D | E |
性质或结构信息 | 其原子核内只有1个质子 | 其单质在空气中体积含量最多 | 其原子M层有3个电子 | 食盐中的金属元素 | 单质在常温、常压下是黄绿色的气体 |
请根据表中的信息回答下列问题:
(1)D离子的结构示意图:___,B原子的电子式:___,E离子的电子式:___。
(2)和B元素的氢化物所含电子数相同的分子有多种,写出任意2种:_________。
(3)A元素与E元素组成的化合物的电离方程式:____。
(4)如图所示为元素周期表中钾元素框图,数据“39.10”表示的是___;写出钾离子的电子式:____。