题目内容
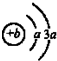 (2012?成都模拟)现有X、Y、Z三种常见短周期元素,x的原子结构示意图如图,Y、Z为同周期金属元素,Y、Z的最高价氧化物对应水化物可以反应生成盐和水.回答下列问题:
(2012?成都模拟)现有X、Y、Z三种常见短周期元素,x的原子结构示意图如图,Y、Z为同周期金属元素,Y、Z的最高价氧化物对应水化物可以反应生成盐和水.回答下列问题:(1)已知Y2 X2为浅黄色固体物质,其阴阳离子个数比为
1:2
1:2
,其中含有的化学键类型有离子键、非极性键
离子键、非极性键
.(2)将单质Z的薄片在酒精灯上加热至熔化,观察到的现象
融化成的小球不落下
融化成的小球不落下
,产生该现象的原因是氧化铝的熔点比铝高
氧化铝的熔点比铝高
.(3)Y、Z最高价氧化物对应的水化物混合反应生成盐和水的离子方程式为
Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
.(4)若(3)中生成物还可表示为YZ(OH)4,则YZ(OH)4与过量HCl溶液反应的离子方程式为
Al(OH)4-+4H+=Al3++4H2O
Al(OH)4-+4H+=Al3++4H2O
.分析:X、Y、Z三种常见短周期元素,由于X的原子结构示意图可知a=2,故X为O元素,结合(1)Y2 X2为浅黄色固体物质,可知Y为Na元素,Y、Z为同周期金属元素,二者的最高价氧化物对应水化物可以反应生成盐和水,为氢氧化钠与氢氧化铝反应,故Z为Al元素,据此解答.
解答:解:X、Y、Z三种常见短周期元素,由于X的原子结构示意图可知a=2,故X为O元素,结合(1)Y2 X2为浅黄色固体物质,可知Y为Na元素,Y、Z为同周期金属元素,二者的最高价氧化物对应水化物可以反应生成盐和水,为氢氧化钠与氢氧化铝反应,故Z为Al元素,
(1)Na2O2由钠离子与过氧根离子构成的离子化合物,其阴阳离子个数比为1:2,过氧根离子与钠离子之间形成离子键,过氧根离子中氧原子之间形成非极性键,故答案为:1:2;离子键、非极性键;
(2)将单质Al的薄片在酒精灯上加热至熔化,由于反应生成氧化铝,氧化铝的熔点比铝高,氧化铝膜兜住铝箔融化成的小球不落下,故答案为:融化成的小球不落下;氧化铝的熔点比铝高;
(3)氢氧化钠与氢氧化铝反应生成偏铝酸钠与水,反应离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)NaAl(OH)4与过量HCl溶液反应生成氯化铝、氯化钠与水,反应离子方程式为:Al(OH)4-+4H+=Al3++4H2O,故答案为:Al(OH)4-+4H+=Al3++4H2O.
(1)Na2O2由钠离子与过氧根离子构成的离子化合物,其阴阳离子个数比为1:2,过氧根离子与钠离子之间形成离子键,过氧根离子中氧原子之间形成非极性键,故答案为:1:2;离子键、非极性键;
(2)将单质Al的薄片在酒精灯上加热至熔化,由于反应生成氧化铝,氧化铝的熔点比铝高,氧化铝膜兜住铝箔融化成的小球不落下,故答案为:融化成的小球不落下;氧化铝的熔点比铝高;
(3)氢氧化钠与氢氧化铝反应生成偏铝酸钠与水,反应离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)NaAl(OH)4与过量HCl溶液反应生成氯化铝、氯化钠与水,反应离子方程式为:Al(OH)4-+4H+=Al3++4H2O,故答案为:Al(OH)4-+4H+=Al3++4H2O.
点评:本题考查元素推断及Na、Al元素化合物的性质等,难度不大,旨在考查学生对基础知识的掌握.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目