题目内容
13.分别用一种试剂将下列物质中混入的少量杂质除去(括号内为混入的杂质)| 物质 | 需加入适量的试剂 | 有关离子方程式 |
| HNO3(H2SO4) | ||
| ZnSO4(CuSO4) | ||
| NaCl(Na2CO3) |
分析 硫酸可与硝酸钡反应生成硫酸钡沉淀和硝酸;可用锌置换出铜;碳酸钠与盐酸反应生成氯化钠和二氧化碳气体,以此解答该题.
解答 解:硫酸可与硝酸钡反应生成硫酸钡沉淀和硝酸,反应的离子方程式为Ba2++SO42-=BaSO4↓;可用锌置换出铜,反应的离子方程式为Zn+Cu2+=Zn2++Cu,碳酸钠与盐酸反应生成氯化钠和二氧化碳气体,反应的离子方程式为2H++CO32-=CO2↑+H2O,
故答案为:
| Ba(NO3)2 | Ba2++SO42-=BaSO4↓ |
| Zn | Zn+Cu2+=Zn2++Cu |
| HCl | 2H++CO32-=CO2↑+H2O |
点评 本题考查物质的分离和除杂,侧重考查元素化合物性质,明确物质性质差异性是解本题关键,注意除杂时不能引进新的杂质,难点是除杂剂的选取,注意把握离子方程式的书写.

练习册系列答案
相关题目
3.下列反应的离子方程式中正确的是( )
| A. | 碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH${\;}_{4}^{+}$+OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| B. | Ca(HCO3)2溶液中滴加少量NaOH溶液 Ca2++HCO3-+OH-=CaCO3↓+H2O | |
| C. | NaHSO4溶液和Ba(OH)2溶液充分反应后溶液呈中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| D. | 向Fe(OH)2中加入稀硝酸:3Fe2++4H++NO${\;}_{3}^{-}$═3Fe3++NO↑+2H2O |
4.化学反应N2(g)+3H2(g)═2NH3(l)的能量变化如图所示,则该反应的△H等于( )


| A. | +2(b-a) kJ•mol-1 | B. | +(b+c-a) kJ•mol-1 | ||
| C. | +(a+b) kJ•mol-1 | D. | +2(a-b-c) kJ•mol-1 |
1.有机物 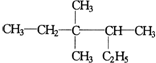 的正确命名为( )
的正确命名为( )
 的正确命名为( )
的正确命名为( )| A. | 2-乙基-3,3-二甲基-4-乙基戊烷 | B. | 3,3-二甲基-4-乙基戊烷 | ||
| C. | 3,3,4-三甲基已烷 | D. | 2,3,3-三甲基已烷 |
8.设NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下22.4L水所含的分子为NA | |
| B. | 16g氧气中所含的电子数为NA | |
| C. | 18g水所含的电子数为8NA | |
| D. | NA个Cl2的质量是71g |
18.下列操作中不正确的是 ( )
| A. | 加热试管内物质时,试管底部与酒精灯外焰接触 | |
| B. | 过滤时,漏斗下方紧贴烧杯内壁 | |
| C. | 过滤时,玻璃棒与三层滤纸的一边接触 | |
| D. | 向试管中滴加液体时,胶头滴管紧贴试管内壁 |
5.和下列离子反应方程式相对应的化学方程式正确的是( )
| A. | Cu2++2OH-═Cu(OH)2CuCO3+2NaOH═Cu(OH)2↓+Na2CO3 | |
| B. | Ba2++SO${\;}_{4}^{2-}$═BaSO4↓ Ba(OH)2+H2SO4═BaSO4↓+2H2O | |
| C. | Ag++Cl-═AgCl↓ AgNO3+NaCl═AgCl↓+NaNO3 | |
| D. | Cu+2Ag+═Cu2++2Ag↓ Cu+2AgCl═2Ag+CuCl2 |
3.已知ag气体X2中含有b个X原子,那么cg该气体在0℃、1.01×105 Pa条件下的体积是(NA 表示阿伏加德罗常数的值)( )
| A. | $\frac{11.2bc}{a{N}_{A}}$ L | B. | $\frac{11.2ab}{c{N}_{A}}$L | C. | $\frac{11.2ac}{b{N}_{A}}$ L | D. | $\frac{11.2b}{ac{N}_{A}}$L |