题目内容
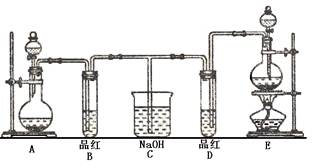
有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如图所示的装置进行实验。通入SO2气体,将带余烬的木条插入试管C中,木条复燃。
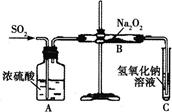
请回答下列问题:
(1)第一小组同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是________________________。
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3__________。
(3) 设计一种实验方案证明Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。为检验是否由Na2SO4生成,他们设计了如下方案:
设计一种实验方案证明Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。为检验是否由Na2SO4生成,他们设计了如下方案:

上述方案是否合理?________ (若不合理,请说明理由;若合理,以下不用回答)
①
②

请回答下列问题:
(1)第一小组同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是________________________。
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3__________。
(3)
 设计一种实验方案证明Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。为检验是否由Na2SO4生成,他们设计了如下方案:
设计一种实验方案证明Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。为检验是否由Na2SO4生成,他们设计了如下方案:
上述方案是否合理?________ (若不合理,请说明理由;若合理,以下不用回答)
①
②
(7分)(1)2Na2O2 + 2SO2 = 2 Na2SO3 +O2 (2分)
(2)取反应生成的白色固体少许,加一定量的稀硫酸,如果产生无色有刺激气味的气体(且能使品红溶液褪色),则说明生成了Na2SO3 (2分)
(3)不合理 (1分)
①稀硝酸能将亚硫酸钡氧化为硫酸钡而不溶解 (1分)
②如果反应后的固体中还残留Na2O2,它溶于水后也能将SO32-氧化成SO42- (1分)
(2)取反应生成的白色固体少许,加一定量的稀硫酸,如果产生无色有刺激气味的气体(且能使品红溶液褪色),则说明生成了Na2SO3 (2分)
(3)不合理 (1分)
①稀硝酸能将亚硫酸钡氧化为硫酸钡而不溶解 (1分)
②如果反应后的固体中还残留Na2O2,它溶于水后也能将SO32-氧化成SO42- (1分)
略

练习册系列答案
相关题目