题目内容
【题目】下列反应在常温下均为非自发反应,在高温下仍为非自发反应的是
A. Ag2O(s)===2Ag(s)+![]() O2(g)
O2(g)
B. Fe2O3(s)+![]() C(s)===2Fe(s)+
C(s)===2Fe(s)+![]() CO2(g)
CO2(g)
C. N2O4(g)===2NO2(g)
D. 6C(s)+6H2O(l)===C6H12O6(s)
【答案】D
【解析】
反应自发进行的判断依据是△H-T△S<0。
A. Ag2O(s)===2Ag(s)+![]() O2(g) 反应的△H>0、△S>0,高温下△H-T△S<0,反应能自发进行,故A错误;
O2(g) 反应的△H>0、△S>0,高温下△H-T△S<0,反应能自发进行,故A错误;
B. Fe2O3(s)+![]() C(s)===2Fe(s)+
C(s)===2Fe(s)+![]() CO2(g) 反应的△H>0、△S>0,高温下△H-T△S<0,反应能自发进行,故B错误;
CO2(g) 反应的△H>0、△S>0,高温下△H-T△S<0,反应能自发进行,故B错误;
C. N2O4(g)===2NO2(g) 反应的△H<0、△S>0,任何情况下△H-T△S<0,反应均能自发进行,故C错误;
D. 6C(s)+6H2O(l)===C6H12O6(s) 反应的△H<0、△S<0,高温下△H-T△S>0,反应不能自发进行,故D正确;
答案选D。

 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案【题目】有关下列四个常用电化学装置的叙述中,正确的是
|
|
|
|
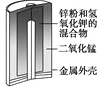
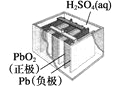
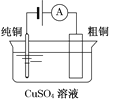
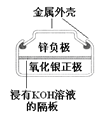
图Ⅰ碱性锌锰电池 | 图Ⅱ铅-硫酸蓄电池 | 图Ⅲ电解精炼铜 | 图Ⅳ银锌纽扣电池 |
A. 图Ⅰ所示电池中,MnO2的作用是催化剂
B. 图Ⅱ所示电池放电过程中,硫酸浓度不断增大
C. 图Ⅲ所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D. 图Ⅳ所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
【题目】已知反应![]() ,某研究小组将4moX和2molY置于一容积不变的密闭容器中,测定一定时间内X的转化率,得到的数据如表所示,下列判断正确的是( )
,某研究小组将4moX和2molY置于一容积不变的密闭容器中,测定一定时间内X的转化率,得到的数据如表所示,下列判断正确的是( )
t/min | 2 | 4.5 | 5 | 6 |
X的转化率 | 30% | 40% | 70% | 70% |
A.随着反应的进行,混合气体的密度不断增大
B.反应在5.5min时,v正(X)=2v逆(Z)
C.6min时,容器中剩余1.4molY
D.其他条件不变,将X的物质的量改为10mol,则可得到4molZ