��Ŀ����
9����״�����Т�6.72L CH4 ��3.01��1023��HCl ��13.6g H2S ��0.2mol NH3�����ж���������Ĺ�ϵ��С�����ʾ����ȷ���ǣ�������| A�� | �ܶ� �٣��ܣ��ۣ��� | B�� | ��ԭ���� �ܣ��ڣ��ۣ��� | ||
| C�� | ���� �ܣ��٣��ۣ��� | D�� | ����ܣ��٣��ۣ��� |
���� ����n=$\frac{V}{{V}_{m}}$����6.72LCH4�����ʵ���������n=$\frac{N}{{N}_{A}}$����HCl�����ʵ���������n=$\frac{m}{M}$����13.6gH2S�����ʵ�����
A����ͬ�����£��ܶ�֮�ȵ���Ħ������֮�ȣ�
B�����ݸ����Ӻ��е�Hԭ����Ŀ����������ʺ��е�Hԭ�����ʵ�����Hԭ�����ʵ���Խ����ԭ����ĿԽ��
C������m=nM������顢HCl�����������������жϣ�
D����ͬ�����£��������֮�ȵ��������ʵ���֮�ȣ�
��� �⣺��6.72LCH4�����ʵ���Ϊ$\frac{6.72L}{22.4L/mol}$=0.3mol����3.01��1023��HCl�����ʵ���Ϊ$\frac{3.01��1{0}^{23}}{6.02��1{0}^{23}mo{l}^{-1}}$=0.5mol����13.6gH2S�����ʵ���Ϊ$\frac{13.6g}{34g/mol}$=0.4mol����0.2molNH3��
A����ͬ�����£��ܶ�֮�ȵ���Ħ������֮�ȣ����ܶȢ٣��ܣ��ۣ��ڣ���A��ȷ��
B��������n��H��=0.3mol��4=1.2mol��HCl��n��H��=0.5mol��������n��H��=0.4mol��2=0.8mol��������n��H��=0.2mol��3=0.6mol����Hԭ����Ŀ�ڣ��ܣ��ۣ��٣���B����
C������m=nM֪����������Ϊ0.3mol��16g/mol=4.8g��HCl������Ϊ0.5mol��36.5g/mol=33.25g������������Ϊ0.2mol��17g/mol=3.4g���������ܣ��٣��ۣ��ڣ���C��ȷ��
D������V=nVm֪����ͬ�����£��������֮�ȵ��������ʵ���֮�ȣ�������ܣ��٣��ۣ��ڣ���D��ȷ��
��ѡB��
���� ���⿼���˰���٤�����ɼ������ۣ���ȷ���ʵ����Ļ�����ʽ�и���������֮��Ĺ�ϵ�ǽⱾ��ؼ�����Ŀ�ѶȲ���

| A�� | ����ϡ��������Ͳ��ȡŨ����ʱ�����ӿ̶��� | |
| B�� | ����Ͳ��ȡ�����Ũ���ᵹ���ձ�������ˮϴ��Ͳ 2��3 �Σ�ϴҺ�����ձ��� | |
| C�� | ���� 11.7 g NaCl ���� 0.2 mol/L NaCl ��Һʱ��������������� | |
| D�� | ����ʱ���ӿ̶��� |
| A�� | n | B�� | $\frac{n}{m}$ | C�� | $\frac{12n}{m}$ | D�� | n��NA |
| A�� | I-��CO32-��SO42- | B�� | SO42-��CO32-��I- | C�� | CO32-��SO42-��I- | D�� | CO32-��I-��SO42- |
��1����֪��2N2H4��l��+N2O4��l���T3N2��g��+4H2O��l����H=-1225kJ��mol-1
| ��ѧ�� | N-H | N-N | N��N | O-H |
| ���ܣ�kJ��mol-1�� | 390 | 190 | 946 | 460 |
��2��800��ʱ��ij�ܱ������д������·�Ӧ��2NO2��g��?2NO��g��+O2��g����H��0������ʼ�������м���1mol/L��NO2����Ӧ������NO�IJ�����ʱ��ı仯��ͼ����I��ʾ��
�ٷ�Ӧ������ڷ�ӦI���ԣ��ı�����������Ǽ��������
������ͼ�л��Ƴ������������뷴ӦI��ͬʱ����Ӧ��820��ʱ���У�NO�IJ�����ʱ��ı仯���ߣ�
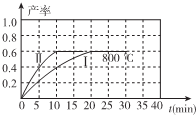
��800��ʱ������ʼʱ��������ͬʱ����1mol/LNO��0.2mol/LO2��0.55mol/L N02����v��������v���棩
��3����֪N2H4��g��?2NO2��g����H=+57.20kJ/mol��tʱ����һ������NO2��N2O4������һ������Ϊ2L�ĺ����ܱ������У�Ũ����ʱ��仯��ϵ���±���ʾ��
| ʱ��/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| c��X��/��mol/L�� | 0.2 | c | 0.6 | 0.6 | 1.0 | c1 | c1 |
| c��Y����mol/L�� | 0.6 | c | 0.4 | 0.4 | 0.4 | c2 | c2 |
��ǰ10min����NO2��ʾ�ķ�Ӧ����Ϊ0.04mol/��L��min����20minʱ�ı������������NO2��Ũ�ȣ����´ﵽƽ��ʱ��NO2�İٷֺ���b����ѡ��ǰ��ĸ����
a������ b����С c������ d�����жϣ�
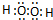 ��
��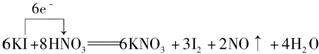 ��
��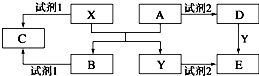 A��B��C��D��E����ѧ��ѧ������5�ֻ��������A��B�����������X��Y�������г����Ľ�����������ʼ��ת����ϵ��ͼ��ʾ�����ַ�Ӧ�����������ȥ����
A��B��C��D��E����ѧ��ѧ������5�ֻ��������A��B�����������X��Y�������г����Ľ�����������ʼ��ת����ϵ��ͼ��ʾ�����ַ�Ӧ�����������ȥ����