题目内容
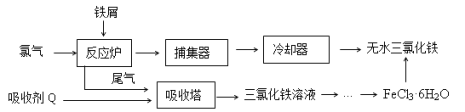
【题目】铝土矿的主要成分中含有氧化铝、氧化铁和二氧化硅等,工业上经过下列工艺可以冶炼金属铝.下列说法不正确的是( )
铝土矿![]() a
a ![]() b
b![]()
![]() c
c![]()
![]() d
d![]() Al.
Al.
A. b中铝元素是以阳离子形式存在
B. ①、②中除加试剂外,还需要进行过滤操作
C. ④进行的操作是加热,而且d一定是氧化铝
D. ③中需要通入过量的二氧化碳
【答案】D
【解析】
A.氧化铝与过量氢氧化钠反应生成偏铝酸钠,然后加入过量盐酸,生成氯化铝,则b中铝元素是以阳离子形式存在,故A正确;
B.①加入氢氧化钠后只有氧化铁不反应,应过滤分离,②中加入过量盐酸,需将氯化铝溶液和硅酸用过滤的方法分离,故B正确;
C.因为电解熔融的氧化铝生成铝,则④进行的操作是加热使氢氧化铝分解为氧化铝,故d一定是氧化铝,C正确;
D.b含有氯化铝,要生成氢氧化铝沉淀,应加入碱性物质,加入二氧化碳实现不了,故D错误.;
本题答案为D。

【题目】1,2-二氯丙烷(CH2ClCHClCH3)是重要的化工原料,工业上可用丙烯加成法生产,主要副产物为3-氯丙烯(CH2=CHCH2C1) ,反应原理为
i.CH2=CHCH,3(g)+Cl2(g)![]() CH2ClCHClCH3(g) ΔH1= -134 kJ mol-1
CH2ClCHClCH3(g) ΔH1= -134 kJ mol-1
ii.CH2=CHCH,3(g)+Cl2(g)![]() CH2=CHCH2Cl (g)+HCl(g) ΔH2= -l02 kJ mol-1
CH2=CHCH2Cl (g)+HCl(g) ΔH2= -l02 kJ mol-1
已知:相关化学键的键能数据如下表所示:
化学键 | C=C | C—C | C—Cl | Cl—Cl |
E/( kJ mol-1) | 611 | x | 328 | 243 |
请回答下列问题:
(1)由反应i计算出表中x=_____________。
(2)一定温度下,密闭容器中发生反应i和反应ii,达到平衡后增大压强,CH2C1CHC1CH3的产率______(填“增大”“减小”或“不变”),理由是_________________________________。
(3)T1℃时,向10L恒容的密闭容器中充入1 mol CH2=CHCH2C1和2 mol HC1,只发生反应CH2=CH CH2Cl (g)+HCl(g)![]() CH2ClCHClCH3(g) ΔH3。 5min反应达到平衡,测得 05 min内,用CH2ClCHClCH3表示的反应速率 v(CH2ClCHClCH3)=0.016 mol·L-1 min-1。
CH2ClCHClCH3(g) ΔH3。 5min反应达到平衡,测得 05 min内,用CH2ClCHClCH3表示的反应速率 v(CH2ClCHClCH3)=0.016 mol·L-1 min-1。
①平衡时,HCl的体积分数为_________(保留三位有效数字)。
②保持其它条件不变,6 min时再向该容器中充入0.6 mol CH2=CHCH2Cl、0.2molHC1和0.1mol CH2ClCHClCH3,则起始反应速率 v正(HCl)___ V逆(HCl) (填“>”“<”或“=”)。