题目内容
【题目】有6种短周期元素,原子序数按E、D、B、A、F、C的顺序依次增大;A、C同周期,B、C同主族;A与B可形成离子化合物A2B,且离子的电子数均相同;D和E可形成4核10电子的分子;F是第三周期元素的简单离子中半径最小的。试回答下列问题(用相应的元素符号表示):
(1)写出B在元素周期表中的位置:__;C的原子结构示意图为__。
(2)B与E形成的化合物E2B2的电子式为__;D和E形成4核10电子的分子的结构式为___;A、B、E形成的化合物中存在的化学键___。
(3)元素A与元素F相比,金属性较弱的是__(用元素符号表示),写出实验室制备其最高价氧化物的水化物反应的离子方程式为__。
【答案】第二周期第ⅥA族 
![]()
![]() 离子键和极性共价键 Al Al3++3NH3H2O=Al(OH)3↓+3NH4+
离子键和极性共价键 Al Al3++3NH3H2O=Al(OH)3↓+3NH4+
【解析】
A与B形成离子化合物A2B,且离子的电子数均相同,说明A在B的下一周期,A显+1价,则A为Na,B显-2价,B为O,B和C同主族,C为S,D和E可形成4核10电子的分子,该分子为NH3,即E为H,D为N,F是第三周期元素的简单离子中半径最小的,即F为Al,据此分析;
A与B形成离子化合物A2B,且离子的电子数均相同,说明A在B的下一周期,D和E可形成4核10电子的分子,该分子为NH3,即E为H,D为N,F是第三周期元素的简单离子中半径最小的,即F为Al, A2B为离子化合物,A显+1价,则A为Na,B显-2价,B为O,B和C同主族,C为S,
(1)B为O,位于第二周期VIA族;C为S,位于第三周期VIA族,原子序数为16,则原子结构示意图为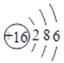 ;
;
(2)E2B2为H2O2,其结构式为H-O-O-H,则H2O2的电子式为![]() ;形成的4核10电子的分子为NH3,空间构型为三角锥,即结构式为
;形成的4核10电子的分子为NH3,空间构型为三角锥,即结构式为![]() ;三种元素形成的化合物为NaOH,NaOH是由Na+和OH-组成,含有化学键为离子键和极性共价键;
;三种元素形成的化合物为NaOH,NaOH是由Na+和OH-组成,含有化学键为离子键和极性共价键;
(3)同周期从左向右金属性逐渐增强,即Na的金属性强于Al;Al元素的最高价氧化物对应水化物为Al(OH)3,Al(OH)3表现两性,实验室常用可溶性铝盐与氨水反应制备氢氧化铝,其离子反应方程式为Al3++3NH3·H2O=Al(OH)3↓+3NH4+。

【题目】有X、Y、Z、T、U五种短周期元素。X、Y、Z 三元素在周期表中的位置如图所示,三元素的原子序数之和是 41。X 和 T 的单质在不同条件下反应,可以生成T2X(白色固体)和T2X2(淡黄色固体)两种化合物。U 单质在 Z 单质中燃烧时产生苍白色火焰,生成物的水溶液能使石蕊试液变红。
X | |
Y | Z |
(1)各元素的符号是 X______,Y______,Z______。
(2)Y 原子的结构示意图为_______。
(3)用电子式表示 Y 与 T 组成的化合物的形成过程:______。
(4)YX2 和 U2Y 反应的化学方程式为______, 其中氧化剂是______,被氧化的元素是______。
【题目】I.(1)实验测得 8 g 液态甲醇(化学式为 CH4O)在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出 181.6 kJ 的热量。请写出表示液态甲醇燃烧热的热化学方程式:_______。
(2)发射卫星时常用肼(N2H4)作为燃料,用二氧化氮作为氧化剂,这两种物质反应生成氮气和水蒸气。 已知:①N2(g)+2O2(g)=2NO2(g) ΔH= a kJ/mol;②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH= b kJ/mol。写出肼气体与二氧化氮气体反应的热化学方程式:_______。
II.某学习小组的同学在实验室利用下图装置进行中和热的测定,请回答下列问题:

(1)在其它操作正确的前提下,如果大烧杯不盖硬纸板,求得的中和热 ΔH 将_______(填“偏大”、“偏小” 或“无影响”)。
(2)取 50 mL 0.50 mol/L NaOH 溶液和 30 mL 0.50 mol/L 硫酸溶液进行实验,实验数据如下表。
实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.5 | 26.7 | 26.6 | 30.1 | |
2 | 26.0 | 26.4 | 26.2 | 30.3 | |
3 | 25.9 | 25.9 | 25.9 | 30.2 | |
4 | 26.4 | 26.2 | 26.3 | 30.5 | |
①表中的温度差的平均值为_____℃。
②近似认为 0.50 mol/L NaOH溶液和 0.50 mol/L硫酸溶液的密度都是 1 g·cm-3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热 ΔH=_____kJ/mol (保留到小数点后一位)。
③实验中改用 60 mL0.50 mol/L 盐酸跟 50 mL 0.55 mol/L 氢氧化钠进行反应,若其它实验操作均正确,则与上述实验相比,所放出的热量_____(填“相等”或“不相等”,下同),所求得的中和热_____。