��Ŀ����
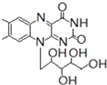
����Ŀ�������������ֿ��������쵼�����״��ֺ��Աʹ�õ�����ƿ���Ʊ�����һ���䷽�к��������������ʣ�
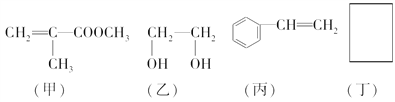
��д���пհף�
��1�����в�����ԭ�ӵĹ�������________�������Լ������Ӧ����ɫ����________(����)��
a��Br2/CCl4��Һ B��ʯ����Һ��c������KMnO4��Һ
��2����ͬ���칹���ж��֣�д������һ�ֲ�����������Ľṹ��ʽ��________��
��3������ͨ������ת�����Եõ���(����A��D��Ϊ�л���)��
����![]() A
A![]() B
B![]() C
C![]() D
D![]() ��
��
A�ķ���ʽ��________���Լ�X������________��
��4�������ﶡ����̼���⡢������Ԫ�أ���Է�������Ϊ110������FeCl3��Һ��������������ɫ���Ҷ������������ϵ�һ��ȡ����ֻ��һ�֡��Ľṹ��ʽΪ________��
���𰸡� ̼̼˫��(��![]() ) a��c CH2=CH��CH2��CH2��COOH C6H12O6 Br2��CCl4��Һ(����ˮ)
) a��c CH2=CH��CH2��CH2��COOH C6H12O6 Br2��CCl4��Һ(����ˮ) ![]()
��������������������⿼������ŵ�ʶ���л�������ʣ���������ͬ���칹�����д���л��ƶϣ��л������ʽ�ͽṹʽ��ȷ����
��1�����еĹ�������̼̼˫����������������ԭ�ӵĹ�����Ϊ̼̼˫����a����к�̼̼˫��������Br2/CCl4��Һ�����ӳɷ�Ӧʹ��Һ��ɫ��b�����ײ���ʹʯ����Һ��ɫ��c�������к�̼̼˫�����ܱ�����KMnO4��Һ������ʹ����KMnO4��Һ��ɫ�����Ӧ����ɫ����a��c����ѡa��c��
��2���Ľṹ��ʽΪ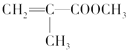 ������ʽΪC5H8O2�������Ͷ�Ϊ2�����в�����������Ľṹ��ʽΪ��CH2=CHCH2CH2COOH��
������ʽΪC5H8O2�������Ͷ�Ϊ2�����в�����������Ľṹ��ʽΪ��CH2=CHCH2CH2COOH��![]() ��
��
��3��������ϡ���ᡢ���������·���ˮ�ⷴӦ���������ǣ�AΪ�����ǣ�A�ķ���ʽΪC6H12O6��A��һ������������B��B��C�ķ�Ӧ������Ũ���ᡢ170����B��CΪ�Ҵ�����ȥ��Ӧ��B�Ľṹ��ʽΪCH3CH2OH��C�Ľṹ��ʽΪCH2=CH2��C![]() D
D![]() �ң��ҵĽṹ��ʽΪ
�ң��ҵĽṹ��ʽΪ![]() �����к�2�����ǻ������Լ�XΪ������Ȼ�̼��Һ����ˮ��D�Ľṹ��ʽΪBrCH2CH2Br��BrCH2CH2Br��NaOH��Һ�м��ȷ���ˮ�ⷴӦ�����ҡ�
�����к�2�����ǻ������Լ�XΪ������Ȼ�̼��Һ����ˮ��D�Ľṹ��ʽΪBrCH2CH2Br��BrCH2CH2Br��NaOH��Һ�м��ȷ���ˮ�ⷴӦ�����ҡ�
��4������FeCl3��Һ��������������ɫ�������ڷ��࣬������Է�������Ϊ110����110-12![]() 6-6-16=16��˵���������л�����1����ԭ�ӣ��������������ϵ�һ��ȡ����ֻ��һ�������Ľṹ�Գƣ���Ϊ�Զ����ӣ��ṹ��ʽΪ
6-6-16=16��˵���������л�����1����ԭ�ӣ��������������ϵ�һ��ȡ����ֻ��һ�������Ľṹ�Գƣ���Ϊ�Զ����ӣ��ṹ��ʽΪ![]() ��
��

����Ŀ�����ڵؿ��еĺ����ϸߣ��輰�仯����Ŀ��������Ѿã����ִ��������й㷺Ӧ�ã��ش��������⣺
��1���մɡ�ˮ��Ͳ����dz��õĴ�ͳ�����ǽ������ϣ�����������ͨ��������Ҫԭ����____________________��
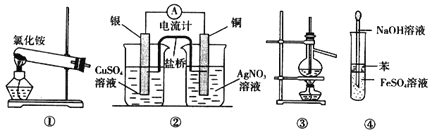
��2���ߴ������ִ���Ϣ���뵼��������Ȳ�ҵ����Ҫ�Ļ������ϣ���ҵ���ᴿ���ж���·�ߣ�����һ�ֹ�������ʾ��ͼ����Ҫ��Ӧ��ͼ��
��п��ԭ���Ȼ�����һ����������Ӧ��ǰ�����Ʊ���ķ��������Ʊ�����ʾ�����£�
![]()
�� ������������Ӧ�Ļ�ѧ����ʽΪ______________________(SiO2+3C![]() SiC+2CO��Ϊ����Ӧ������Ʒ�е��ʹ���̼��������ʵ���֮��Ϊ1��1����μӷ�Ӧ��C��SiO2������֮��Ϊ________________��
SiC+2CO��Ϊ����Ӧ������Ʒ�е��ʹ���̼��������ʵ���֮��Ϊ1��1����μӷ�Ӧ��C��SiO2������֮��Ϊ________________��
�������Ʊ����̱����ϸ������ˮ��SiCl4��ˮ����ˮ�����������ᣬ��Ӧ�Ļ�ѧ����ʽ��_________________________��
�� ��ҵ��Ҳ����ͨ������ͼ��ʾ��������ȡ���裺

���й����ʵķе��������±����ᴿSiHCl3����Ҫ���ղ��������dz�����������_________��SiHCl3����ˮ�⣬����ȫˮ��Ļ�ѧ����ʽΪ___________________________��
���� | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
�е�/�� | 2355 | 57.6 | 31.8 | 8.2 | ��30.4 | ��84.9 | ��111.9 |
�� ����ÿһ�ִ��Ʊ�1mol���裬�����������й�Ԫ��û����ʧ����ӦI��HCl��������Ϊ90%����ӦII��H2��������Ϊ93.75%�����ڵڶ��ִε������У�����Ͷ��HCl ��H2�����ʵ���֮����___________________��