籾朕坪否
‐籾朕/壓炎彈彜趨和嗤⦿〙6.72LCH4⇧〖3.01〜1023倖HCl蛍徨⇧〗13.6gH2S⇧∠0.2molNH3。和双斤宸膨嶽賑悶議宙峰屎鳩議頁( )
a. 悶持〖﹅〗﹅〙﹅∠ b. 畜業〖﹅〗﹅∠﹅〙
c. 嵎楚〖﹅〗﹅〙﹅∠ d. 狽圻徨倖方〙﹅〗﹅∠﹅〖
A. abc B. bcd C. abd D. abcd
‐基宛/D
‐盾裂/
編籾a、遮莱議悶持頁6⤴72L⇧3⤴01〜1023倖HCl蛍徨議悶持=11⤴2L⇧13⤴6g H2S議悶持=![]() 〜22⤴4L/mol=8⤴96L⇧0⤴2mol NH3議悶持=0⤴2mol〜22⤴4L/mol=4⤴48L⇧侭參賑悶悶持寄弌乏會頁〖﹅〗﹅〙﹅∠⇧a屎鳩◉ b⤴屢揖訳周和⇧賑悶彫櫛悶持屢揖⇧功象ρ=
〜22⤴4L/mol=8⤴96L⇧0⤴2mol NH3議悶持=0⤴2mol〜22⤴4L/mol=4⤴48L⇧侭參賑悶悶持寄弌乏會頁〖﹅〗﹅〙﹅∠⇧a屎鳩◉ b⤴屢揖訳周和⇧賑悶彫櫛悶持屢揖⇧功象ρ=![]() 岑⇧畜業嚥凪屢斤蛍徨嵎楚撹屎曳⇧侭參畜業寄弌乏會頁〖﹅〗﹅∠﹅〙⇧b屎鳩◉c、遮莱議嵎楚頁
岑⇧畜業嚥凪屢斤蛍徨嵎楚撹屎曳⇧侭參畜業寄弌乏會頁〖﹅〗﹅∠﹅〙⇧b屎鳩◉c、遮莱議嵎楚頁![]() =4.8g、3.01〜1023倖HCl蛍徨議麗嵎議楚頁0.5mol⇧嵎楚頁0.5mol〜36.5g/mol=18.25g、〗H2S議嵎楚頁13.6g、∠0.2 mol NH3議嵎楚頁0.2mol〜17g/mol=3.4g⇧嵎楚〖﹅〗﹅〙﹅∠⇧c屎鳩◉d、遮莱議麗嵎議楚
=4.8g、3.01〜1023倖HCl蛍徨議麗嵎議楚頁0.5mol⇧嵎楚頁0.5mol〜36.5g/mol=18.25g、〗H2S議嵎楚頁13.6g、∠0.2 mol NH3議嵎楚頁0.2mol〜17g/mol=3.4g⇧嵎楚〖﹅〗﹅〙﹅∠⇧c屎鳩◉d、遮莱議麗嵎議楚![]() ⇧根狽圻徨1.2mol◉〖3.01〜1023倖HCl蛍徨⇧根嗤狽圻徨0.5mol◉〗13.6 g H2S麗嵎議楚
⇧根狽圻徨1.2mol◉〖3.01〜1023倖HCl蛍徨⇧根嗤狽圻徨0.5mol◉〗13.6 g H2S麗嵎議楚![]() =0.425mol⇧根狽圻徨倖0.85mol◉∠0.2 mol NH3⇧根狽圻徨倖0.6mol◉狽圻徨倖方〙﹅〗﹅∠﹅〖⇧d屎鳩;絞僉D。
=0.425mol⇧根狽圻徨倖0.85mol◉∠0.2 mol NH3⇧根狽圻徨倖0.6mol◉狽圻徨倖方〙﹅〗﹅∠﹅〖⇧d屎鳩;絞僉D。

 堋響酔概狼双基宛
堋響酔概狼双基宛‐籾朕/嬬坿頁繁窃慌揖購廣議嶷勣諒籾。匈冫賑頁貫匈冫蚊嶄蝕寡竃栖議匯嶽掲械嶷勣議爺隼賑彿坿⇧匈冫賑議麼勣撹蛍頁遮莱⇧頁巷範議準昌嬬坿。
↙1⇄匈冫賑音叙嬬喘恬伴創⇧珊辛喘噐伏恢栽撹賑(CO才H2)。CH4嚥H2O(g)宥秘詔醜湊剩嬬郡哘匂⇧窟伏郡哘 CH4(g)+H2O(g)=CO(g)+3H2(g)@H1
厮岑⦿〙CH4、H2、CO 議伴付犯↙@H⇄蛍艶葎-a kJmol-1、-b kJmol-1、-c kJmol-1◉
〖H2O (l) =H2O(g)◉ @H=+dkJmol-1
夸@H1= ___________↙喘根忖銚a、b、c、d議旗方塀燕幣⇄kJmol-1。
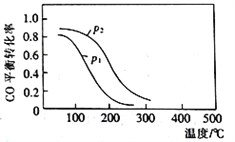
↙2⇄喘栽撹賑伏撹遮桓議郡哘葎⦿CO(g)+2H2(g)![]() CH3OH(g) @H2⇧壓10L冴否畜液否匂嶄梓麗嵎議楚岻曳1|2割秘CO才H2⇧霞誼CO議峠財廬晒楕嚥梁業才儿膿議購狼泌和夕侭幣⇧200≧扮n(H2)昧扮寂議延晒泌和燕侭幣⦿
CH3OH(g) @H2⇧壓10L冴否畜液否匂嶄梓麗嵎議楚岻曳1|2割秘CO才H2⇧霞誼CO議峠財廬晒楕嚥梁業才儿膿議購狼泌和夕侭幣⇧200≧扮n(H2)昧扮寂議延晒泌和燕侭幣⦿
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
〙@H2_________ (野^> ̄^< ̄賜^ =  ̄)0。
〖和双傍隈屎鳩議頁____________ (野炎催⇄。
a.梁業埆互⇧乎郡哘議峠財械方埆寄
b.器峠財朔壅割秘蓮嗤賑悶⇧CO議廬晒楕戻互
c.否匂坪賑悶儿膿音壅延晒扮⇧郡哘器欺恷寄尫業
d.夕嶄儿膿p1<p2
〗 03 min坪喘CH3OH燕幣議郡哘堀楕v(CH3OH)=________mol L-1,min-1。
∠ 200≧扮⇧乎郡哘議峠財械方K =_______。﨑貧峰200≧器欺峠財議冴否畜液否匂嶄壅紗秘2 mol CO、2 mol H2、2 mol CH3OH⇧隠隔梁業音延⇧夸晒僥峠財____________(野^屎﨑 ̄、^剃﨑 ̄賜^音 ̄)卞強。
↙3⇄遮莱、剳賑才KOH卑匣辛怏撹伴創窮学。炎彈彜趨和宥秘5.6 L遮莱⇧霞誼窮揃嶄廬卞1.2 mol窮徨⇧夸遮莱議旋喘楕葎_________。