题目内容
【题目】把镁铝合金用稀硫酸溶解,加入氢氧化钠溶液的体积与生成沉淀的质量关系如右图,则合金中镁和铝的质量比是( ) 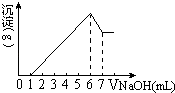
A.1:1
B.8:9
C.4:3
D.4:9
【答案】B
【解析】解:设NaOH的浓度为cmol/L,合金中Al的物质的量为x,Mg的物质的量为y,
由6~7mL发生的反应为Al(OH)3+NaOH═NaAlO2+2H2O,则
Al~Al(OH)3~ | NaOH |
1 | 1 |
x | (7﹣6)×0.001L×c |
x=0.001cmol,
由1~6mL发生Al3++3OH﹣═Al(OH)3↓、Mg2++2OH﹣═Mg(OH)2↓,则
Al3++ | 3OH﹣═Al(OH)3↓ |
1 | 3 |
0.001cmol | 0.003cmol |
Mg2++ | 2OH﹣═Mg(OH)2↓ |
1 | 2 |
y | (0.005c﹣0.003c)mol |
y=0.001cmol,
则合金中镁和铝的质量比为0.001cmol×24g/mol:0.001cmol×27g/mol=8:9,
故选B.
【考点精析】通过灵活运用铝的化学性质,掌握很快与O2反应,形成致密氧化膜,抗腐蚀性比镁强;在纯氧中或高温下可燃烧;与沸水只有微弱反应即可以解答此题.

练习册系列答案
相关题目