题目内容
下列有关含铜化合物的说法错误的是(设NA为阿伏加德罗常数的值)
| A.用盐酸可以洗去铜表面的铜锈 |
| B.0.1mol/L的CuSO4溶液中,Cu2+的数目一定小于0.1NA |
| C.在CuCl2和FeCl3的混合溶液中加入铁粉,若有固体残留,则其中一定含有铜 |
| D.在FeSO4溶液中加入CuS固体,溶液中c(Fe2+)不变,说明Ksp(CuS)远小于Ksp(FeS) |
B
试题分析:A、铜锈的主要成分是碱式碳酸铜,所以可用盐酸可以洗去铜表面的铜锈,A正确;B、由于不能确定硫酸铜溶液的体积,因此0.1mol/L的CuSO4溶液中,Cu2+的数目不一定小于0.1NA,B不正确;C、铁离子的氧化性强于铜离子,所以在CuCl2和FeCl3的混合溶液中加入铁粉,铁首先与铁离子发生氧化还原反应,然后再与铜离子发生置换反应。因此若有固体残留,则其中一定含有铜,C正确;D、在FeSO4溶液中加入CuS固体,溶液中c(Fe2+)不变,说明不能生成硫化亚铁。因此根据沉淀容易向更难溶的方向转化可知Ksp(CuS)远小于Ksp(FeS),D正确,答案选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
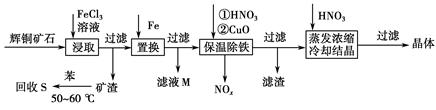
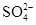 生成,可向溶液中滴加Ba(NO3)2溶液
生成,可向溶液中滴加Ba(NO3)2溶液 样品含有少量
样品含有少量 杂质。现要测定其中
杂质。现要测定其中 的质量分数,实验按以下步骤进行:
的质量分数,实验按以下步骤进行:

 溶液18.00mL。该样品中
溶液18.00mL。该样品中