题目内容
【题目】分子式为C5H12O的醇中,能被氧化为酮的有
A. 2种B. 3种C. 4种D. 5种
【答案】B
【解析】
能被氧化铜氧化成酮为醇,与-OH相连的C上只有1个H,据此分析。
能被氧化铜氧化成酮为醇,与-OH相连的C上只有1个H,分子式为C5H12O的醇与-OH相连的C上只有1个H的有CH3CH2CH2CH(OH)CH3、CH3CH(OH)CH2(CH3)2、CH3CH2CH(OH)CH2CH3共3种,故符合条件的3种。
答案选B。

【题目】KMnO4是中学化学常见的试剂。
Ⅰ.某小组拟用酸性KMnO4溶液与H2C2O4(弱电解质)的反应来探究“外界条件对化学反应速率的影响”,并设计了如下的方案记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20mol/L H2C2O4溶液、0.010mol/L KMnO4酸性溶液、蒸馏水、试管、量筒、秒表、恒温水浴槽
物理量 编号 | V(0.20 mol/L H2C2O4溶液)/mL | 甲 | V(0.010mol/L KMnO4溶液)/mL | M(MnSO4固体)/g | T/℃ | 乙 |
① | 2.0 | 0 | 4.0 | 0 | 50 | |
② | 2.0 | 0 | 4.0 | 0 | 25 | |
③ | 1.0 | a | 4.0 | 0 | 25 | |
④ | 2.0 | 0 | 4.0 | 0.1 | 25 |
回答下列问题:
(1)完成上述反应原理的离子反应方程式________
![]()
(2)上述实验①②是探究________对化学反应速率的影响;若上述实验②③是探究浓度对化学反应速率的影响,则表格中“甲”应填写________,a为________;
乙是实验需要测量的物理量,则表格中“乙”应填写________。
上述实验②④是探究________对化学反应速率的影响。
Ⅱ.某化学小组利用下图装置进行实验证明氧化性:KMnO4>Cl2>Br2。限选试剂:KBr溶液、KMnO4溶液、浓盐酸、浓硫酸
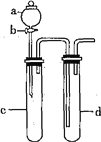
(3)装置a、d中盛放的试剂分别是:________、________;
(4)实验中观察到的现象为________________________________;
此实验装置的不足之处是____________________。
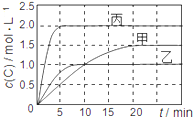
【题目】向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g)![]() 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和下图表示:
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和下图表示:
容器 | 甲 | 乙 | 丙 |
容积 | 1L | 1L | 2L |
温度 | T1 | T2 | T2 |
反应物 起始量 | 1molA 2molB | 1molA 2molB | 4molA 8molB |
下列说法正确的是 ( )
A. 由图可知:T1<T2,且该反应为吸热反应
B. T1时该反应的平衡常数K=7.2
C. 前10min甲、乙、丙三个容器中A的平均反应速率:v(A)乙<v(A)甲<v(A)丙
D. 平衡时A的质量m:m乙<m甲<m丙