题目内容
某稀溶液中含4molKNO3和2.5molH2SO4,向其中加入1.5molFe粉,充分反应后产生的气体在标况下的体积为( )
A.36L B.28L C.22.4L D.11.2L
B
【解析】
试题分析:因为硝酸有强氧化性,铁没有过量的情况下,没机会成生亚铁。
反应如下:
Fe + 4HNO3 = Fe(NO3)3 + NO↑ + H2O
如果铁过量,有机会发生:
Fe + 2Fe(NO3)3 = 3Fe(NO3)2
题目中,整个过程都是发生:
Fe + 4HNO3 = Fe(NO3)3 + NO↑ + H2O--------(1)这个反应的。
根据题目中硝酸钾与硫酸的量,可知,溶液中有4摩尔硝酸。
第一次反应,4摩尔硝酸与1摩尔铁反应,生成1摩尔硝酸铁和1摩尔NO。
生成的1摩尔硫酸铁与剩余的1摩尔氢离子又得到1摩尔的硝酸,再与剩下的0.5摩尔铁,再发生:
Fe + 4HNO3 = Fe(NO3)3 + NO↑ + H2O--------(2)
因为硝酸只有1摩尔,又没有氢离子补充,所以(2)这个反应,只有0.25摩尔铁参加,再生成0.25摩尔NO.
这样气体总物质的量生成1.25mol ,体积是28升。
然后剩余的0.25mol铁,与硝酸铁再发生:
Fe + 2Fe(NO3)3 = 3Fe(NO3)2这个反应。
反应到此结束.
考点:硝酸的氧化性
点评:此题要注意反应的实质。是硝酸根和氢离子与金属的反应。只要能提供硝酸根和氢离子反应就能进行。

 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案I.下图为向25mL0.1mol/L NaOH溶液中逐滴滴加0.2moL/L CH3COOH溶液过程中溶液pH的变化曲线
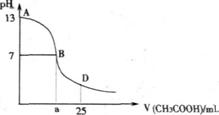 |
请回答:
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确? (选填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间内还是BD区间内? (若正确,此问不答)
(2)关于该滴定实验,从下列选项中选出最恰当的一项
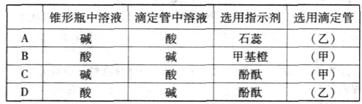
(3)在AB区间内,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)的大小关系是
A.c(OH-)一定大于c(CH3COO-)
B.c(OH-)一定小于c(CH3COO-)
C.c(OH-)一定等于c(CH3COO-)
D.c(OH-)可能大于、小于或等于C(CH3COO-)
(4)在D点时,溶液中c(CH3COO-)+c(CH3COOH) 2c(Na+)。(填“>”、“<”或“=”)
Ⅱ.在温度t℃时,某NaOH稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,则:
(5)该温度下水的离子积常数Kw=
(6)该NaOH稀溶液中NaOH物质的量浓度的精确值是 mol/L(用含字母的表达式表示)
(7)在该温度下(t℃),将100mL 0.1mol/L的稀H2SO4溶液与100mL0.4mol/L的NaOH溶液混合后,溶液的pH=