题目内容
下列说法中,不正确的是
- A.10g H218O与0.5mol D2O所含中子数相等
- B.等物质的量的甲基(-CH3)与羟基(-OH)所含质子数相等
- C.等物质的量的OH-与NH4+所含电子数与质子数均相等
- D.标准状况下,以任意比例混合的CH4和CO2混合物22.4L,含有的分子数为NA
C
分析:A.利用n= 及物质的构成来解答;
及物质的构成来解答;
B.1mol甲基中含有9mol质子,1mol羟基中含有9mol质子;
C.1mol OH-中质子为9mol,电子为10mol;1molNH4+中质子为11mol,电子为10mol;
D.标准状况下,以任意比例混合的CH4和CO2混合物22.4L,其物质的量为1mol.
解答:A.10gH218O中的中子为 ×(0+10)=5mol,0.5mol D2O所含中子为0.5mol×(1×2+8)=5mol,故A正确;
×(0+10)=5mol,0.5mol D2O所含中子为0.5mol×(1×2+8)=5mol,故A正确;
B.1mol甲基中含有1mol×(6+3)=9mol质子,1mol羟基中含有1mol×(8+1)=9mol质子,故B正确;
C.1mol OH-中质子为9mol,电子为10mol;1mol NH4+中质子为11mol,电子为10mol,则质子数不同,故C错误;
D.标准状况下,以任意比例混合的CH4和CO2混合物22.4L,由n=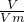 ,N=nNA可知,含有的分子数为NA,故D正确;
,N=nNA可知,含有的分子数为NA,故D正确;
故选C.
点评:本题考查物质的量的有关计算,明确以物质的量为中心的计算公式及原子的构成即可解答,难度不大.
分析:A.利用n=
 及物质的构成来解答;
及物质的构成来解答;B.1mol甲基中含有9mol质子,1mol羟基中含有9mol质子;
C.1mol OH-中质子为9mol,电子为10mol;1molNH4+中质子为11mol,电子为10mol;
D.标准状况下,以任意比例混合的CH4和CO2混合物22.4L,其物质的量为1mol.
解答:A.10gH218O中的中子为
 ×(0+10)=5mol,0.5mol D2O所含中子为0.5mol×(1×2+8)=5mol,故A正确;
×(0+10)=5mol,0.5mol D2O所含中子为0.5mol×(1×2+8)=5mol,故A正确;B.1mol甲基中含有1mol×(6+3)=9mol质子,1mol羟基中含有1mol×(8+1)=9mol质子,故B正确;
C.1mol OH-中质子为9mol,电子为10mol;1mol NH4+中质子为11mol,电子为10mol,则质子数不同,故C错误;
D.标准状况下,以任意比例混合的CH4和CO2混合物22.4L,由n=
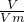 ,N=nNA可知,含有的分子数为NA,故D正确;
,N=nNA可知,含有的分子数为NA,故D正确;故选C.
点评:本题考查物质的量的有关计算,明确以物质的量为中心的计算公式及原子的构成即可解答,难度不大.

练习册系列答案
相关题目
 C60的发现导致了一门新兴学科--碳球化学的兴起.根据对其分子结构特点的研究,科学家预测,C60的很多化合物可能在超导体、长效药物载体等方面有着重要的应用.目前已证明,C60与金属钾作用得到一种物质K3C60,其在低温下具有超导性能.下列说法中,不正确的是( )
C60的发现导致了一门新兴学科--碳球化学的兴起.根据对其分子结构特点的研究,科学家预测,C60的很多化合物可能在超导体、长效药物载体等方面有着重要的应用.目前已证明,C60与金属钾作用得到一种物质K3C60,其在低温下具有超导性能.下列说法中,不正确的是( )| A、C60是一种含碳化合物 | B、在C60和 K3C60中,碳元素分别以游离态和化合态存在 | C、K3C60是一种新型的化合物 | D、C60是碳元素的一种单质 |
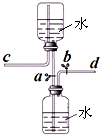 如图是某同学设计的储气装置(固定装置已略去),下列说法中,不正确的是( )
如图是某同学设计的储气装置(固定装置已略去),下列说法中,不正确的是( )