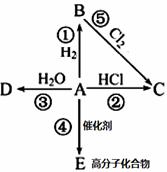
��Ŀ����
ij�����ĵ�������к���ͭ�����Ƚ��������Ϊʵ����Դ�Ļ������ò���Ч��ֹ������Ⱦ��������¹������̣�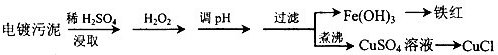
��1����������H2O2��Ŀ����______����pH�����м�����Լ������______���ѧʽ����ʵ���ҽ��й��˲������õ��IJ���������______��
��2�����CuSO4��Һ��ԭ����______����CuSO4��Һ�м���һ������NaCl��Na2SO3���������ɰ�ɫ��CuCl������д���÷�Ӧ�Ļ�ѧ����ʽ______��
��3��CuCl��Ʒ��CuCl��������������96.50%Ϊ���Һϸ������ȡ���Ʊ���CuCl��Ʒ0.2500g����һ������0.5mol?L-1FeCl3��Һ�У�����Ʒ��ȫ�ܽ��ˮ20mL����0.1000mol?L-1��Ce��SO4��2��Һ�ζ��������յ�ʱ����Ce��SO4��2��Һ24.60mL���йصĻ�ѧ��ӦΪ��Fe3++CuCl=Fe2++Cu2++Cl-��Ce4++Fe2+=Fe3++Ce3+��ͨ������˵����CuCl��Ʒ______������ϡ������ϡ������ұ���
��4��25��ʱ��KSP[Fe��OH��3]=4.0��10-38��Fe3+����ˮ�ⷴӦFe3++3H2O?Fe��OH��3+3H+���÷�Ӧ��ƽ�ⳣ��Ϊ______��
| ������ | Fe��OH��3 | Fe��OH��2 | Cu��OH��2 |
| ��ʼ������pH | 2.3 | 7.6 | 4.4 |
| ��ȫ������pH | 3.2 | 9.7 | 6.4 |
��2�����CuSO4��Һ��ԭ����______����CuSO4��Һ�м���һ������NaCl��Na2SO3���������ɰ�ɫ��CuCl������д���÷�Ӧ�Ļ�ѧ����ʽ______��
��3��CuCl��Ʒ��CuCl��������������96.50%Ϊ���Һϸ������ȡ���Ʊ���CuCl��Ʒ0.2500g����һ������0.5mol?L-1FeCl3��Һ�У�����Ʒ��ȫ�ܽ��ˮ20mL����0.1000mol?L-1��Ce��SO4��2��Һ�ζ��������յ�ʱ����Ce��SO4��2��Һ24.60mL���йصĻ�ѧ��ӦΪ��Fe3++CuCl=Fe2++Cu2++Cl-��Ce4++Fe2+=Fe3++Ce3+��ͨ������˵����CuCl��Ʒ______������ϡ������ϡ������ұ���
��4��25��ʱ��KSP[Fe��OH��3]=4.0��10-38��Fe3+����ˮ�ⷴӦFe3++3H2O?Fe��OH��3+3H+���÷�Ӧ��ƽ�ⳣ��Ϊ______��
��1����������к���ͭ�����Ƚ���������������Ҫ���ܽ�ͭ�����Ƚ��������˫��ˮ��ǿ�����ԣ���������ԭ�Ե����ʣ�Fe2+���л�ԭ�ԣ���������H2O2��Fe2+�ܱ�˫��ˮ����Ϊ�����ӣ����ڵ���pHֵ��
Cu2+���룬��pH�����м�����Լ�����Ǽ���ij�����ʳ�ȥ��Һ�е����Ҳ������µ����ʣ�����Ҫ��������ͭ����������ͭ��̼��ͭ������Һ��pHֵ4.4ʱ��ͭ���ӿ�ʼ���ֳ���������Һ��pHֵΪ3.2ʱ�����������ӳ�����ȫ��ͭ����δ��������������Ҫʹ���������Ӻ�ͭ���ӷ��룬���˲����õ�������������̨��©�����ձ����������ȣ��������ڲ��������У�©�����ձ�����������
�ʴ�Ϊ����Fe2+������Fe3+�����ڵ���pHֵ��Cu2+���룻CuO����Cu��OH��2����CuCO3��©�����ձ�����������
��2�������������ʱȽ��ȶ��������ȵ�153������ҵķֽ�Ϊˮ������������Һ�й�����H2O2��ȥ�ɼ������б���Ӱ����һ��CuCl�����ɣ���ΪCuSO4��+2�۵�ͭ�ܰ�Na2SO3��+4�۵���������+6�۵�����CuSO4��Һ�м���һ������NaCl��Na2SO3ʱ���ɰ�ɫ��CuCl��������Ӧ�Ļ�ѧ����ʽΪ��2CuSO4+2NaCl+Na2SO3+H2O=2CuCl��+2Na2SO4+H2SO4��
�ʴ�Ϊ��������Һ�е�H2O2������Ӱ����һ��CuCl�����ɣ�2CuSO4+2NaCl+Na2SO3+H2O=2CuCl��+2Na2SO4+H2SO4��
��3������Ʒ��CuCl������Ϊx���йصĻ�ѧ��ӦΪ��Fe3++CuCl=Fe2++Cu2++Cl-��Ce4++Fe2+=Fe3++Ce3+����
�ɻ�ѧ��Ӧ����ʽ��֪��CuCl������Fe2+������Ce4+
11
n��CuCl��24.60��10-3L��0.1000mol/L
����n��CuCl��=24.60��10-3L��0.1000mol/L=2.46��10-3mol��
���Ը���ƷCuCl������Ϊ2.46��10-3mol��99.5g/mol=0.2448g��
0.2500g�ϸ��CuCl�к���CuCl������0.2500g��96.5%=0.2413g��С��0.2448g�����Ը���Ʒ��CuCl�������������ϱ���
�ʴ�Ϊ�����ϣ�
��4��Ksp[Fe��OH��3]=c��Fe3+����c3��OH-��=4.0��10-38��c��H+��=
����Ӧ
Fe3++3H2O?Fe��OH��3+3H+��ƽ�ⳣ��K=
�T
=2.5��10-5��
�ʴ�Ϊ��2.5��10-5��
Cu2+���룬��pH�����м�����Լ�����Ǽ���ij�����ʳ�ȥ��Һ�е����Ҳ������µ����ʣ�����Ҫ��������ͭ����������ͭ��̼��ͭ������Һ��pHֵ4.4ʱ��ͭ���ӿ�ʼ���ֳ���������Һ��pHֵΪ3.2ʱ�����������ӳ�����ȫ��ͭ����δ��������������Ҫʹ���������Ӻ�ͭ���ӷ��룬���˲����õ�������������̨��©�����ձ����������ȣ��������ڲ��������У�©�����ձ�����������
�ʴ�Ϊ����Fe2+������Fe3+�����ڵ���pHֵ��Cu2+���룻CuO����Cu��OH��2����CuCO3��©�����ձ�����������
��2�������������ʱȽ��ȶ��������ȵ�153������ҵķֽ�Ϊˮ������������Һ�й�����H2O2��ȥ�ɼ������б���Ӱ����һ��CuCl�����ɣ���ΪCuSO4��+2�۵�ͭ�ܰ�Na2SO3��+4�۵���������+6�۵�����CuSO4��Һ�м���һ������NaCl��Na2SO3ʱ���ɰ�ɫ��CuCl��������Ӧ�Ļ�ѧ����ʽΪ��2CuSO4+2NaCl+Na2SO3+H2O=2CuCl��+2Na2SO4+H2SO4��
�ʴ�Ϊ��������Һ�е�H2O2������Ӱ����һ��CuCl�����ɣ�2CuSO4+2NaCl+Na2SO3+H2O=2CuCl��+2Na2SO4+H2SO4��
��3������Ʒ��CuCl������Ϊx���йصĻ�ѧ��ӦΪ��Fe3++CuCl=Fe2++Cu2++Cl-��Ce4++Fe2+=Fe3++Ce3+����
�ɻ�ѧ��Ӧ����ʽ��֪��CuCl������Fe2+������Ce4+
11
n��CuCl��24.60��10-3L��0.1000mol/L
����n��CuCl��=24.60��10-3L��0.1000mol/L=2.46��10-3mol��
���Ը���ƷCuCl������Ϊ2.46��10-3mol��99.5g/mol=0.2448g��
0.2500g�ϸ��CuCl�к���CuCl������0.2500g��96.5%=0.2413g��С��0.2448g�����Ը���Ʒ��CuCl�������������ϱ���
�ʴ�Ϊ�����ϣ�
��4��Ksp[Fe��OH��3]=c��Fe3+����c3��OH-��=4.0��10-38��c��H+��=
| 10-14 |
| c(OH-) |
Fe3++3H2O?Fe��OH��3+3H+��ƽ�ⳣ��K=
| c3(H+) |
| c(Fe3+) |
| 10-42 |
| c(Fe3+)?c3(OH-) |
�ʴ�Ϊ��2.5��10-5��

��ϰ��ϵ�д�
�����Ŀ
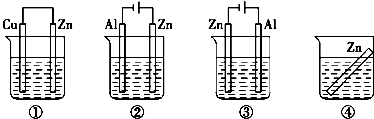
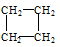 ��
��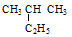 ������ ������ ��
������ ������ ��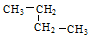 �����л�Ϊͬ���칹����� ������ţ��������֮��Ĺ�ϵΪ ��
�����л�Ϊͬ���칹����� ������ţ��������֮��Ĺ�ϵΪ ��