题目内容
【题目】火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当把 0.4mol 液态肼和 0.8mol H2O2 混合反应,生成氮气和水蒸气,放出 256.7kJ 的热量(相当于 25°C、101kPa下测得的热量)。(注:所有数值均保留小数点后一位)
(1)写出肼的结构式:_____________,过氧化氢电子式_____________。
(2)反应的热化学方程式为______________________________。
(3)已知 H2O(l)=H2O(g)ΔH=+44kJ/mol.则 16g 液态肼与液态双氧水反应生成液态水时放出的热量是_________ kJ。
【答案】 ![]()
![]() N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)ΔH=-641.8kJ/mol 408.9
N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)ΔH=-641.8kJ/mol 408.9
【解析】本题主要考查反应热的计算。
(1)肼的结构式: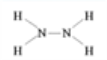 ,过氧化氢电子式:
,过氧化氢电子式:![]() 。
。
(2)反应的热化学方程式为N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)ΔH=-641.8kJ/mol。
(3)已知H2O(l)=H2O(g)ΔH=+44kJ/mol,则16g即0.5mol液态肼与液态双氧水反应生成2mol液态水时放出的热量是641.8/2+2×44kJ=408.9kJ。

练习册系列答案
相关题目
