题目内容
碱式次氯酸镁[Mga(ClO)b(OH)c·xH2O]是一种有开发价值的微溶于水的无机抗菌剂。为确定碱式次氯酸镁的组成,进行如下实验:
① 准确称取1.685g碱式次氯酸镁试样于250mL锥形瓶中,加入过量的KI溶液,用足量乙酸酸化,用O.8000mol/LNa2S2O3标准溶液滴定至终点(离子方程式为2S2O32-+I2=2I-+S4O62-),消耗25.00mL。
② 另取1.685g碱式次氯酸镁试样,用足量乙酸酸化,再用足量3%H2O2溶液处理至不再产生气泡(H2O2被ClO-氧化为O2),稀释至1000mL。移取25.00mL溶液至锥形瓶中,在一定条件下用0.020 00mol/L EDTA(Na2H2Y)标准溶液滴定其中的Mg2+(离子方程式为Mg2++H2Y2-=MgY2-+2H+) ,消耗25.00 mL
(1)步骤① 中需要用到的指示剂是_______。
(2)步骤② 中若滴定管在使用前未用EDTA标准溶液润洗,测得的Mg2+物质的量将____(填“偏高”、“偏低”或“不变”)。
(3)通过计算确定碱式次氯酸镁的化学式(写出计算过程)。____
练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目
下列实验操作和理象、结论均正确且有因果关系的是
选项 | 实验操作和现象 | 结论 |
A | 向某溶液中滴加CCl4,振荡、静置,下层溶液显紫色 | 原溶液中含有I- |
B | 常温下,0.1mol/LNaHSO3溶液的pH约为5 | HSO3-的电离程度大于其水解程度 |
C | 相同温度下,测得饱和亚硫酸溶液的pH小于饱和碳酸溶液的pH | 亚硫酸的酸性强于碳酸 |
D | 向稀HNO3中加入过量的Fe粉,充分反应后,滴入KSCN溶液不显红色 | 稀HNO3将Fe氧化为Fe2+ |
A. A B. B C. C D. D


 3Fe(s)+4 CO2(g),阻碍循环反应的进行。
3Fe(s)+4 CO2(g),阻碍循环反应的进行。

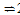 3FeO(s) + CO2(g)平衡常数的变化趋势是________;(填“增大”、“减小”或“不变”)1040℃时,该反应的化学平衡常数的数值是________。
3FeO(s) + CO2(g)平衡常数的变化趋势是________;(填“增大”、“减小”或“不变”)1040℃时,该反应的化学平衡常数的数值是________。

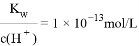 的溶液中:Na+、Fe3+、I-、AlO2-
的溶液中:Na+、Fe3+、I-、AlO2-