题目内容
向2 L密闭容器中通入6mol气体A和6mol气体B,在一定条件下发生反应:
xA(g)+yB(g)=pC(g)+qD(g) 已知:平均反应速率v(C)=1/2v(A);反应2 min时,A的浓度减少了1mol/L,B的物质的量减少了3mol,有6mol D生成。回答下列问题:
(1)反应2 min内,v(A)= ,v(B)= ;
(2)该反应化学方程式中x:y:p:q= ;
(3)如果其他条件不变,将容器的容积变为1 L,进行同样的实验,则与上述反应比较:反应速率 (填“增大”、“减小”或“不变”),理由是 。
xA(g)+yB(g)=pC(g)+qD(g) 已知:平均反应速率v(C)=1/2v(A);反应2 min时,A的浓度减少了1mol/L,B的物质的量减少了3mol,有6mol D生成。回答下列问题:
(1)反应2 min内,v(A)= ,v(B)= ;
(2)该反应化学方程式中x:y:p:q= ;
(3)如果其他条件不变,将容器的容积变为1 L,进行同样的实验,则与上述反应比较:反应速率 (填“增大”、“减小”或“不变”),理由是 。
(1)0.50mol/(L·min),0.75mol/(L·min)
(2)2:3:1:6
(3)增大;体积减小,物质的量浓度变大,反应物浓度越大,反应越快。
(2)2:3:1:6
(3)增大;体积减小,物质的量浓度变大,反应物浓度越大,反应越快。
试题分析:(1)反应2 min内,A的浓度减少了1mol/L,B的物质的量减少了1.5mol/L,所以v(A)=1mol/L/2min=0.50mol/(L·min),v(B)=1.5mol/L/2min="0.75" mol/(L·min);
(2)因为v(C)=1/2v(A),所以v(C)=0.25 mol/(L·min),D的浓度增加3mol/L,所以v(D)=1.5 mol/(L·min),根据化学反应速率之比等于方程式中化学计量数之比,所以
x:y:p:q=0.5:0.75:0.25:1.5=2:3:1:6
(3)体积减小,反应物的浓度增大,反应物浓度越大,反应越快,所以反应速率增大。

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
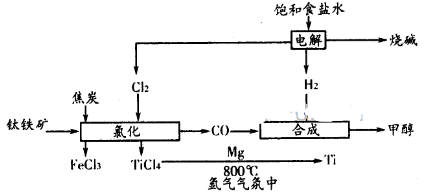
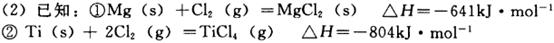
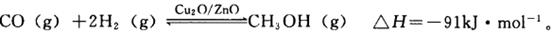
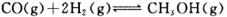 的化学平衡常
的化学平衡常 。
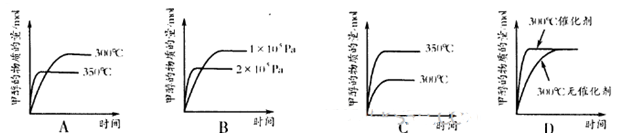
。
 2NH3(g) ΔH<0,反应过程如图:下列说法正确的是
2NH3(g) ΔH<0,反应过程如图:下列说法正确的是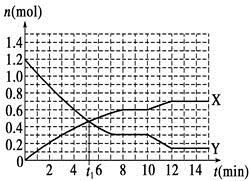
 C(g),经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确的是
C(g),经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确的是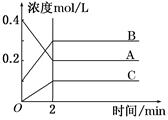
 2B(g)+C(g)
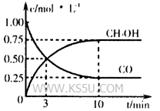
2B(g)+C(g) CH3OH(g)。请根据图示回答下列问题:
CH3OH(g)。请根据图示回答下列问题:
 4NO2(g)+O2(g) ΔH>0。反应物和部分生成物的物质的量随反应时间变化的曲线如图所示。下列说法中不正确的是( )
4NO2(g)+O2(g) ΔH>0。反应物和部分生成物的物质的量随反应时间变化的曲线如图所示。下列说法中不正确的是( )