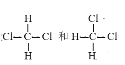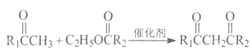题目内容
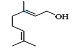
【题目】雾霾天气给人们的出行及身体造成了极大的危害。研究![]() 、
、![]() 、
、![]() 等大气污染气体的处理具有重要意义。
等大气污染气体的处理具有重要意义。
(1)利用钠碱循环法可脱除烟气中的![]() 。
。
①在钠碱循环法中,![]() 溶液作为吸收液,可由
溶液作为吸收液,可由![]() 溶液吸收
溶液吸收![]() 制得,该反应的离子方程式是____。
制得,该反应的离子方程式是____。
②吸收液吸收![]() 的过程中,
的过程中,![]() 随
随![]() 变化关系如下表:
变化关系如下表:
|
| 1∶1 |
|
|
|
|
|
由上表判断,![]() 溶液显______性(填“酸”、“碱”或“中”),用化学平衡原理解释:______。
溶液显______性(填“酸”、“碱”或“中”),用化学平衡原理解释:______。
③当吸收液的![]() 降至约为6时,需送至电解槽再生。再生示意图如下:
降至约为6时,需送至电解槽再生。再生示意图如下:

写出![]() 在阳极放电的电极反应式:________________,当阴极室中溶液
在阳极放电的电极反应式:________________,当阴极室中溶液![]() 升至8以上时,吸收液再生并循环利用。
升至8以上时,吸收液再生并循环利用。
(2)用![]() 催化还原
催化还原![]() 可以消除氮氧化物的污染。例如:
可以消除氮氧化物的污染。例如:
![]()
![]()
![]()
![]()
若用标准状况下![]() 还原
还原![]() 至
至![]() ,整个过程中转移的电子总数为______(阿伏加德罗常数的值用
,整个过程中转移的电子总数为______(阿伏加德罗常数的值用![]() 表示),放出的热量为______
表示),放出的热量为______![]() 。
。
(3)工业上合成氨所需氢气的制备过程中,其中的一步反应为:
![]()
![]()
一定条件下,将![]() 与
与![]() 以体积比为
以体积比为![]() 置于密闭容器中发生上述反应,达到平衡时测得
置于密闭容器中发生上述反应,达到平衡时测得![]() 与
与![]() 体积比为1∶6,则平衡常数
体积比为1∶6,则平衡常数![]() ______。
______。
【答案】2OH-+SO2=SO32-+H2O 酸性 HSO3-存在电离平衡HSO3-H++SO32- 和水解平衡HSO3-+H2OH2SO3+OH-,HSO3-的电离程度大于水解程度 HSO3-+H2O-2e-=SO42-+3H+ 1.6NA 173.4 ![]()
【解析】
(1)①二氧化硫和氢氧化钠反应生成亚硫酸钠和水,注意弱电解质写化学式;②根据溶液中亚硫酸氢根离子浓度和亚硫酸根离子浓度的相对大小确定溶液的酸碱性;③阳极上HSO3-失电子发生氧化反应;
(2)利用盖斯定律计算反应热;
(3)根据反应前和反应后一氧化碳和水之间的体积比结合反应方程式计算出平衡时各种物质的物质的量浓度,再根据平衡常数公式进行计算。
(1)①酸性氧化物和碱反应生成盐和水,所以二氧化硫和氢氧化钠反应生成亚硫酸钠和水,反应的离子方程式为2OH-+SO2=SO32-+H2O,故答案为:2OH-+SO2=SO32-+H2O;
②在亚硫酸氢钠溶液中主要以HSO3-存在,HSO3-的电离很微弱,所以n(SO32-)∶n(HSO3-)1∶1,根据表格知,当亚硫酸氢根离子的物质的量大于亚硫酸根离子的物质的量时,亚硫酸氢钠溶液呈酸性,亚硫酸氢根离子在溶液中既存在水解平衡又存在电离平衡,亚硫酸氢钠溶液呈酸性说明HSO3-的电离程度大于水解程度,故答案为:酸性;HSO3-存在电离平衡HSO3-H++SO32- 和水解平衡HSO3-+H2OH2SO3+OH-,HSO3-的电离程度大于水解程度;
③根据图示,阳极上亚硫酸氢根离子失电子和水反应生成硫酸根离子和氢离子,电极反应式为:HSO3-+H2O-2e-=SO42-+3H+,故答案为:HSO3-+H2O-2e-=SO42-+3H+;
(2)已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol,②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ/mol,利用盖斯定律将![]() 得CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g);△H=-867kJ/mol;1molCH4反应转移8mol电子,n(CH4)=
得CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g);△H=-867kJ/mol;1molCH4反应转移8mol电子,n(CH4)=![]() =0.2mol,整个过程中转移的电子总数为0.2mol×8NA /mol =1.60NA,放出的热量为0.2mol×867kJ/mol=173.4kJ,故答案为:1.6NA;173.4;
=0.2mol,整个过程中转移的电子总数为0.2mol×8NA /mol =1.60NA,放出的热量为0.2mol×867kJ/mol=173.4kJ,故答案为:1.6NA;173.4;
(3)设加入的一氧化碳的物质的量浓度为amol/L,则H2O(g)的物质的量浓度为2amol/L,假设平衡时一氧化碳的物质的量浓度为xmol/L,H2O(g)的物质的量浓度为6xmol/L
CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
开始(mol/L) a 2a 0 0
反应(mol/L) a-x 2a-6x a-x a-x
平衡(mol/L) x 6x a-x a-x
则(a-x)∶(2a-6x)=1∶1,解得:x=0.2amol/L,所以平衡时,c(CO)=0.2amol/L,c(H2O)=1.2amol/L,c(H2)=c(CO2)=0.8amol/L,K=![]() =
=![]() ,故答案为:
,故答案为:![]() 。
。