题目内容
【题目】已知某铁盐含三种元素,为了探究其组成并将之转化为硫酸铁,设计了如下实验:
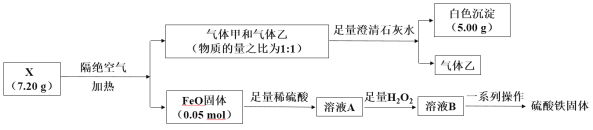
请回答:
(1)铁盐X的化学式为________________,气体乙的化学式为________________。
(2)写出溶液A中加入H2O2后发生反应的离子方程式______________________。
(3)由溶液B制备纯净硫酸铁的一系列操作为:蒸发浓缩、______、过滤、洗涤、干燥。
(4)为确保溶液A到B反应完全,需要检验B溶液中有无Fe2+残留,请设计简单的实验:__________________________。
【答案】FeC2O4 CO 2Fe2++H2O2+2H+=2Fe3++2H2O 冷却结晶或冷却热饱和溶液 取少量B溶液,滴入KMnO4溶液,若紫色变浅褪去,说明仍有Fe2+,反之则无
【解析】
由转化关系可知X在隔绝空气下加热生成FeO,且生成气体甲可使澄清石灰水变浑浊,应为CO2,则X含有Fe、C、O三种元素,则生成的乙为CO,且n(CO)=c(CO2)=n(CaCO3)=![]() =0.05mol,满足m(FeO)+m(CO)+m(CO2)= 0.05mol×72g/mol+0.05mol×28g/mol +0.05mol×44g/mol =7.20g,因此n(Fe):n(C):n(O)=0.05∶0.1∶(0.05+2×0.05+0.05)=1∶2∶4,则X的化学式为FeC2O4,以此解答该题。
=0.05mol,满足m(FeO)+m(CO)+m(CO2)= 0.05mol×72g/mol+0.05mol×28g/mol +0.05mol×44g/mol =7.20g,因此n(Fe):n(C):n(O)=0.05∶0.1∶(0.05+2×0.05+0.05)=1∶2∶4,则X的化学式为FeC2O4,以此解答该题。
(1)由以上分析可知X为FeC2O4,气体乙为CO,故答案为:FeC2O4;CO;
(2)溶液A含有硫酸亚铁,具有还原性,加入H2O2后发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O,故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(3)B为硫酸铁,由溶液B制备纯净硫酸铁的一系列操作为:蒸发浓缩、冷却结晶、过滤、洗涤、干燥,故答案为:冷却结晶;
(4)为确保溶液A到B反应完全,需要检验B溶液中有无Fe2+残留,可利用亚铁离子的还原性,可取少量B溶液,滴入KMnO4溶液,若紫色变浅甚至褪去,说明仍有Fe2+,反之则没有亚铁离子,故答案为:取少量B溶液,滴入KMnO4溶液,若紫色变浅褪去,说明仍有Fe2+,反之则无。

 53随堂测系列答案
53随堂测系列答案