题目内容
【题目】某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示。下列判断正确的是
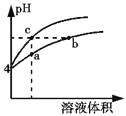
A. a、c两点溶液的导电能力相同
B. a、b、c三点溶液中水的电离程度:a>b>c
C. b点溶液中:c(H+)+c(NH3·H2O)=c(OH—)
D. 用等浓度NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液体积Vb=Vc
【答案】B
【解析】试题分析:氯化氢为强电解质,溶于水全部电离,溶液中的氢离子主要是盐酸电离出来的;氯化铵为强酸弱碱盐,氢离子来自铵离子的水解,水解是微弱的,pH相同的盐酸和氯化铵溶液,氯化铵的浓度远大于盐酸的浓度;体积和pH都相同的盐酸和氯化铵溶液加水稀释的过程中,盐酸不能继续电离,盐酸中氢离子浓度变化大;氯化铵溶液中铵离子的水解平衡正向移动,溶液中氢离子浓度变化小,所以含c点的曲线pH变化是盐酸的,含a、b点的曲线pH变化是氯化铵溶液的。A、溶液的导电能力取决于溶液中自由移动离子的浓度,起始氯化铵的浓度远大于盐酸的浓度,稀释相同的倍数还是氯化铵的浓度远大于盐酸的浓度,故导电能力:a点大于c点,A错误;B、盐酸电离出的氢离子浓度抑制水的电离,所以c点溶液中水的电离程度最小;水解促进水的电离,由于氯化铵溶液中的氢离子浓度来自于铵根离子水解生成的氢离子,氢离子浓度越大,说明水解程度越大,水的电离程度越大,a点的pH<b点的pH,说明a点氢离子大于b点氢离子,a、b二点溶液水的电离程度:a>b,综上所述a、b、c三点溶液水的电离程度a>b>c,B正确;C、根据质子守恒知,b点溶液中c(OH-)+c(NH3H2O)=c(H+),C错误;D、用等浓度NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液体积Vb>Vc,D错误。答案选B。

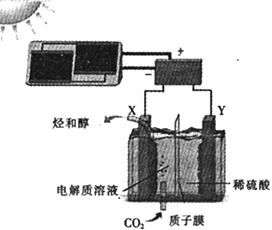
【题目】【加试题】甲醇水蒸气重整制氢(SRM)是用于驱动电动汽车的质子交换膜燃料电池的理想氢源,当 前研究主要集中在提高催化剂活性和降低尾气中CO含量,以免使燃料电池Pt电极中毒。重整过程发生的反应如下:
反应I CH3OH(g)+H2O(g) ![]() CO2(g)+3H2(g) ΔH1
CO2(g)+3H2(g) ΔH1
反应Ⅱ CH3OH(g) ![]() CO(g)+2H2(g) ΔH2
CO(g)+2H2(g) ΔH2
反应Ⅲ.CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
其对应的平衡常数分别为K1、K2、K3,其中K2、K3随温度变化如下表所示:
125℃ | 225℃ | 325℃ | |
K2 | 0.5535 | 185.8 | 9939.5 |
K3 | 1577 | 137.5 | 28.14 |
请回答:
(1)反应Ⅱ能够自发进行的条件_______ (填 “低温”、“高温”或“任何温度”), ΔH1____ΔH3 (填 “>”、“<”或 “=” )。
(2)相同条件下,甲醇水蒸气重整制氢较甲醇直接分解制氢(反应Ⅱ)的先进之处在于_________。
(3)在常压、CaO催化下,CH3OH和H2O混和气体(体积比1∶1.2,总物质的量2.2mol)进行反应,tl时刻测得 CH3OH转化率及CO、CO2选择性随温度变化情况分别如图所示(CO、CO2的选择性:转化的CH3OH中生成CO、CO2的百分比)。

注:曲线a表示CH3OH的转化率,曲线b表示CO的选择性,曲线c表示 CO2的选择性
① 下列说法不正确的是_____。
A.反应适宜温度为300℃
B.工业生产通 常在负压条件下进行甲醇水蒸气重整
C.己知 CaO催化剂具有更高催化活性,可提高甲醇平衡转化率
D.添加CaO的复合催化剂可提高氢气产率
② 260℃ 时H2物质的量随时间的变化曲线如图所示。画出300℃时至t1时刻H2物质的量随时间的变化曲线_____。
(4)副产物CO2可以在酸性水溶液中电解生成甲酸,生成甲酸的电极反应式是_________。