题目内容
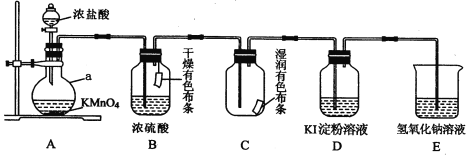
【题目】某化学兴趣小组用下图装置制取并探究氯气的性质。
A装置中发生反应的化学方程式: KMnO4+ HCl(浓) == KCl+ MnCl2 + Cl2↑+ H2O,____________
(1)制取氯气反应中MnCl2是__________ 产物(填“氧化”或“还原”)。
(2)实验进行一段时间后,可观察到______(填“B”或“C”)装置中有色布条褪色,其褪色原因是______________________________________。
(3)当氯气进入D装置后,可观察到溶液颜色变为_____________,写出相关反应的化学方程式___________________________________。
(4)写出E装置中反应的离子方程式___________________________。
(5)用31.6 g KMnO4固体与足量的浓盐酸反应,最多可生成标准状况下_________L氯气。被氧化的HCl的物质的量是___________。
(6)若氯气泄漏,某同学用湿毛巾捂住鼻子防止中毒,有以下四种溶液可浸湿毛巾,它们分别是:①NaOH溶液②NaHCO3溶液③KBr溶液④NaCl溶液,正确选择是______(填序号)。
【答案】2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O 还原 C 氯气与水反应生成漂白性物质(HClO) 蓝色 Cl2+2KI=I2+2KCl Cl2+2OH-=Cl-+ClO-+H2O 11.2 1mol ②
【解析】
根据反应中Mn和Cl元素的化合价变化情况结合守恒法配平反应的方程式。
(1)根据化学反应前后Mn元素价态分析判断;
(2)依据Cl2本身不具有漂白性,但是Cl2与H2O反应生成的HClO具有漂白性来分析;
(3)氯气具有强氧化性,能够氧化碘离子生成单质碘,碘遇到淀粉变蓝;
(4)氯气有毒不能直接排放到空气中;
(5)根据n=m÷M结合反应的方程式计算;
(6)用湿毛巾捂住鼻子防止中毒,应选弱碱性物质吸收氯气。
反应中Mn元素化合价从+7价降低到+2价,得到5个电子,氯元素化合价从-1价升高到0价,失去1个电子,则根据电子得失守恒以及原子守恒可知反应的方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O;
(1)由方程式2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O得反应前后Mn元素价态降低,因此KMnO4是氧化剂,所以MnCl2是还原产物;
(2)因为干燥的Cl2本身不具有漂白性,不能将有色物质褪色,故B中干燥布条不变色,C中湿润的布条有水,氯气与水反应生成的HClO具有漂白性能将有色物质褪色,故C中褪色;
(3)氯气具有强氧化性,能够氧化碘离子生成单质碘,化学方程式为Cl2+2KI=I2+2KCl,碘遇到淀粉变蓝,所以会看到溶液变蓝;
(4)氯气是有毒气体,不能直接排放到空气中,因此用碱液吸收,所以E装置中反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O;
(5)n(KMnO4)=31.6g÷158g/mol=0.2mol,根据方程式2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O可知生成氯气是0.5mol,在标况下的体积是0.5mol×22.4L/mol=11.2L;根据氯原子守恒可知被氧化的氯化氢是0.5mol×2=1mol;
(6)用湿毛巾捂住鼻子防止中毒,应选弱碱性物质吸收氯气,只有②符合,而①碱性太强,③反应生成有毒物质溴,④抑制氯气溶解,故答案为②。

 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案