题目内容
【题目】示踪原子法是研究化学反应的重要方法之一,下列化学方程式正确的是
A. 2Na2O2+2H218O= 4NaOH+18O2 ↑
B. 2KMnO4+5H218O +3H2SO4= K2SO4+2MnSO4+ 518O2↑+8H2O
C. CH3C18OOH + CH3OH![]() CH3CO18OCH3+H2O
CH3CO18OCH3+H2O
D. 6H37Cl+ NaClO3==NaCl+37Cl2+3H2O
【答案】B
【解析】A、氧气中的氧来源于过氧化钠:2Na2O2+2H218O= 2Na18OH+O2 ↑+2NaOH,故A错误;B、2KMnO4+5H218O2 +3H2SO4= K2SO4+2MnSO4+ 518O2↑+8H2O,过氧化氢跟酸性高锰酸钾溶液反应,过氧化氢中的-1的O被氧化,生成0价的氧气,故B正确;C、在浓硫酸存在条件下与足量乙酸充分反应,化学方程式为:CH3C18OOH + CH3OH![]() CH3C18OOCH3+H2O,故C错误;D、氯酸钠跟浓盐酸混合,氯酸钠中的氯被还原,生成氯气,即37Cl应在氯气中,反应为 6H37Cl+ NaClO3==Na37Cl+3Cl2(537Cl-Cl)+3H2O,故D错误;故选B。
CH3C18OOCH3+H2O,故C错误;D、氯酸钠跟浓盐酸混合,氯酸钠中的氯被还原,生成氯气,即37Cl应在氯气中,反应为 6H37Cl+ NaClO3==Na37Cl+3Cl2(537Cl-Cl)+3H2O,故D错误;故选B。

 金钥匙试卷系列答案
金钥匙试卷系列答案【题目】某研究性学习小组同学为了探究“在相同的温度和压强下、相同体积的任何气体都含有相同数目和分子”,他们设计了如下实验装置并记录相关实验数据。实验装置:
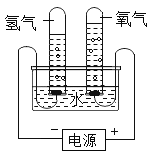
部分实验数据:
温度 | 压强 | 时间 | 水槽中H2O的质量 | H2体积 | O2体积 |
30℃ | 101 kPa | 0 | 300 g | 0 | 0 |
30℃ | 101 kPa | 4分钟 | 298.2 g | 1.243 L |
请回答下列问题:
(1)4分钟时H2、O2物质的量分别是__________mol、___________mol。
(2)该温度下,气体摩尔体积是________________。
(3)假设电解H2O速率相同,2分钟时试管内收集到的H2的体积是___________mL。
(4)根据以上实验得出如下结论,其中不正确的是_________________。
A. 气体摩尔体积与气体的温度相关
B. 在该实验条件下,3 mol O2的气体摩尔体积为74.58 L/mol
C. 同温、同压下,2 mol O2和2 mol CO和CO2混合气体的体积相同
D. 该实验条件下,O2的密度为1.287 g/L