��Ŀ����
����Ŀ��ʵ���ҿ������̿���Ҫ�ɷ�ΪMnO2���Ʊ�KMnO4���������£����̿����������KOH��KClO3�ڸ����·�Ӧ����������أ�K2MnO4����KCl����ˮ�ܽ⣬��ȥ��������Һ�ữ��K2MnO4ת��ΪMnO2��KMnO4����ȥMnO2������Ũ����Һ���ᾧ�õ�����ɫ����״KMnO4����ش�
��1�����̿��Ʊ�K2MnO4�Ļ�ѧ����ʽ��_______________________��
��2��K2MnO4�Ʊ�KMnO4�����ӷ���ʽ��_______________��
��3������2.5g���̿�MnO2 80������������ʵ�飬KMnO4�����۲���Ϊ_______________��
��4��KMnO4�����ȵľ������ữ��Na2C2O4��Һ��Ӧ����Mn2+��CO2���÷�Ӧ�Ļ�ѧ����ʽ��________________________��
��5�������Ƶ�KMnO4��Ʒ0.165g��ǡ����0.335g Na2C2O4��Ӧ��ȫ����KMnO4�Ĵ���Ϊ___��
���𰸡�(12��)(1��3MnO2+6KOH+KClO3![]() 3K2MnO4+KCl+3H2O(2��)
3K2MnO4+KCl+3H2O(2��)
��2��3Mn![]() +4H+ = MnO2��+2Mn
+4H+ = MnO2��+2Mn![]() +2H2O(2��)
+2H2O(2��)
��3��������������ѧ����ʽ��֪����Ӧ����������ļ�����ϵΪ��(3��)
![]()
![]() MnO2K2MnO4
MnO2K2MnO4![]() KMnO4
KMnO4
87 158��![]()
2.5��80% x
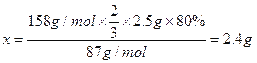
��KMnO4�����۲�����2.4g
��4��2KMnO4+5Na2C2O4+8H2SO4![]() K2SO4+2MnSO4+5Na2SO4+10CO2��+8H2O(2��)
K2SO4+2MnSO4+5Na2SO4+10CO2��+8H2O(2��)
��5�����KMnO4�Ĵ���Ϊy�����ݻ�ѧ����ʽ��֪(3��)
![]() KMnO4������Na2C2O4
KMnO4������Na2C2O4
![]() ��158 134
��158 134
0.165 �� y 0.335
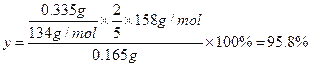
����������