题目内容
【题目】某硝酸厂处理尾气中NO的方法是在催化剂存在时用H2将NO还原为N2:NO(g)+H2(g)=== ![]() N2(g)+H2O(g) ΔH=m kJ·mol-1,其能量变化过程如下:
N2(g)+H2O(g) ΔH=m kJ·mol-1,其能量变化过程如下:
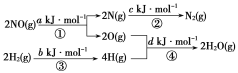
下列说法正确的是( )
A.过程①②③④都是放热过程
B.m=+![]() (a+b-c-d)
(a+b-c-d)
C.m=-![]() (c+a-d-b)
(c+a-d-b)
D.m=![]() (c+d-a-b)
(c+d-a-b)
【答案】B
【解析】分子变为原子需要吸收能量,原子结合为分子释放出能量,则有:2NO(g)===2N(g)+2O(g) ΔH1=+a kJ·mol-1①、2N(g)===N2(g) ΔH2=-c kJ·mol-1②、2H2(g)===4H(g) ΔH3=+b kJ·mol-1③、2O(g)+4H(g)===2H2O(g) ΔH4=-d kJ·mol-1④。根据盖斯定律,由①+②+③+④得2NO(g)+2H2(g)===N2(g)+2H2O(g) ΔH=+(a+b-c-d)kJ·mol-1,则NO(g)+H2(g)=== ![]() N2(g)+H2O(g) ΔH=+
N2(g)+H2O(g) ΔH=+![]() (a+b-c-d)kJ·mol-1,故选B。
(a+b-c-d)kJ·mol-1,故选B。

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目


