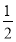题目内容
在100 ℃时,将0.40 mol二氧化氮气体充入2 L密闭容器中,每隔一段时间对该容器内
的物质进行分析,得到如下数据:
时间(s) | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
下列说法中正确的是( )
A.反应开始20 s内以二氧化氮表示的平均反应速率为0.001 25 mol·L-1·s-1
B.80 s时混合气体的颜色与60 s时相同,比40 s时的颜色深
C.80 s时向容器中加入0.32 mol氦气,同时将容器扩大为4 L,则平衡将不移动
D.若起始投料为0.20 mol N2O4,相同条件下达平衡,则各组分含量与原平衡体系对应相等
D
【解析】发生反应2NO2(g)  N2O4(g),前20 s内v(N2O4)=
N2O4(g),前20 s内v(N2O4)= =0.001 25 mol·L-1·
=0.001 25 mol·L-1·
s-1,v(NO2)=0.002 5 mol·L-1·s-1,A错误。60 s、80 s时n(NO2)=0.24 mol,比40 s时的浓度小,颜色浅,B错误。容器体积增大,压强减小,平衡向逆反应方向移动,C错误。

练习册系列答案
相关题目