题目内容
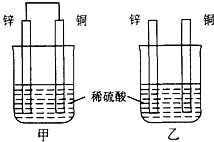
在铜锌硫酸原电池中,锌为______极,______电子,电极发生的是______反应(填氧化或还原),电极反应式为______;铜为______极,______电子,电极发生的是______反应,电极反应式为______,铜片上观察到的现象为______.
铜、锌、稀硫酸构成的原电池中,锌易失电子发生氧化反应而作负极,负极上电极反应式为 Zn-2e-=Zn2+;铜作正极,正极上氢离子得电子发生还原反应,电极反应式为2H++2e-=H2↑,铜电极上有氢气生成,所以看到的现象是铜片上有气泡产生,
故答案为:负;失;氧化;Zn-2e-=Zn2+;正;得;还原;2H++2e-=H2↑;有气泡产生.
故答案为:负;失;氧化;Zn-2e-=Zn2+;正;得;还原;2H++2e-=H2↑;有气泡产生.

练习册系列答案
相关题目