题目内容
【题目】在下列化学方程式中标出电子转移的方向和数目,并回答下列问题
![]() 浓
浓![]() ______ ,其中氧化剂为 ______ 还原剂为 ______ 还原产物为 ______ 氧化产物为 ______
______ ,其中氧化剂为 ______ 还原剂为 ______ 还原产物为 ______ 氧化产物为 ______
![]() ______ ,若有1mol
______ ,若有1mol![]() 生成,则被还原的
生成,则被还原的![]() 是 ______ mol,转移 ______ mol电子。
是 ______ mol,转移 ______ mol电子。
【答案】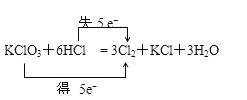
![]() HCl
HCl ![]()
![]()
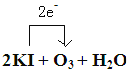
![]() 2
2
【解析】
![]() 浓
浓![]() 中,Cl元素的化合价由
中,Cl元素的化合价由![]() 价升高为0,Cl元素的化合价由
价升高为0,Cl元素的化合价由![]() 价降低为0,该反应转移
价降低为0,该反应转移![]() ;
;
![]() ,I元素的化合价由
,I元素的化合价由![]() 价升高为0,O元素的化合价由0降低为
价升高为0,O元素的化合价由0降低为![]() 价,该反应转移
价,该反应转移![]() ,以此来解答。
,以此来解答。
![]() 浓
浓![]() 中,Cl元素的化合价由
中,Cl元素的化合价由![]() 价升高为0,还原剂为HCl,被氧化,则氧化产物为,Cl元素的化合价由
价升高为0,还原剂为HCl,被氧化,则氧化产物为,Cl元素的化合价由![]() 价降低为0,氧化剂为
价降低为0,氧化剂为![]() ,被还原,还原产物为
,被还原,还原产物为![]() ,该反应转移
,该反应转移![]() ,即电子转移的方向和数目为
,即电子转移的方向和数目为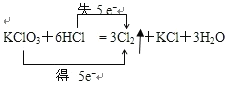 ;
;
故答案为: ;
;![]() ;HCl;
;HCl;![]() ;
;![]() ;
;
![]() 的反应中,I元素的化合价升高,O元素的化合价降低,转移电子为
的反应中,I元素的化合价升高,O元素的化合价降低,转移电子为![]() ,则有1mol
,则有1mol![]() 生成,转移2mol电子,参加反应的
生成,转移2mol电子,参加反应的![]() 为1mol,由电子守恒可知,被还原的
为1mol,由电子守恒可知,被还原的![]() 是
是![]() ,单线桥标出电子转移的方向和数目为
,单线桥标出电子转移的方向和数目为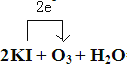 ;
;
故答案为;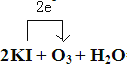 ;
;![]() ;2。
;2。

练习册系列答案
相关题目