题目内容
(1)已知:
Fe(s)+1/2O2(g)=FeO(s) ΔH=-272.0 kJ·mol-1
2Al(s)+3/2O2(g)=Al2O3(s) ΔH=-1675.7 kJ·mol-1
Al和FeO发生铝热反应的热化学方程式是________.
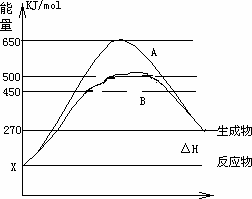
(2)反应物与生成物均为气态的某可逆反应在不同条件下的反应历程分别为A、B,如下图所示.
①
据图判断该反应是________(填“吸”或“放”)热反应,当反应达到平衡后,其他条件不变,升高温度,反应物的转化率________(填“增大”、“减小”或“不变”)②
其中B历程表明此反应采用的条件为________(选填下列序号字母)A.升高温度
B.增大反应物的浓度
C.降低温度
D.使用了催化剂
(3)1000℃
时,硫酸钠与氢气发生下列反应:Na2SO4(s)+4H2(g)①该反应的平衡常数表达式为________.已知K1000℃<K1200℃,则该反应是________反应(填“吸热”或“放热”).
②用有关离子方程式说明上述反应所得固体产物的水溶液的酸碱性________
(4)常温下
,如果取0.1 mol·L-1HA溶液与0.1 mol·L-1 NaOH溶液等体积混合(混合后溶液体积的变化忽略不计),测得混合液的pH=8,请回答下列问题:①
混合溶液中水电离出的c(H+)与0.1 mol·L-1 NaOH溶液中水电离出的c(H+)比较________(填<、>、=).②
已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH________7(填<、>、=);相同温度下,等物质的量浓度的下列盐溶液按pH由大到小的排列顺序为________.(填序号)a.NH4HCO3
b.NH4A
c.(NH4)2CO3
d.NH4Cl
答案:
解析:
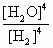 (2分) 吸热;(1分)
(2分) 吸热;(1分)
解析:
(1)3FeO(s)+2Al(s)=Al2O3(s)+3Fe(s) ΔH=-859.7 kJ/mol(2分)
(2)①
吸(1分) 增大(1分)②D(1
分)(3)①K=
②S2-+H2O![]() HS-+OH-(2
HS-+OH-(2
(4)①>(2分)
②>(2
分) c>a>b>d(2分)
练习册系列答案
相关题目
 (2010?潍坊一模)铁元素及其化合物与人类的生产生活息息相关,
(2010?潍坊一模)铁元素及其化合物与人类的生产生活息息相关,